
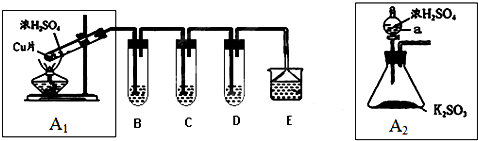
分析 (1)B、C、D分别检验SO2的漂白性、还原性和氧化性,实验室用品红溶液检验漂白性,碘具有氧化性,可以检验二氧化硫的还原性;硫化氢具有还原性,可以检验二氧化硫的氧化性;碘和二氧化硫、水反应生成硫酸、HI;
(2)A2装置不用加热、易于控制反应速率.
解答 解:(1)B、C、D分别检验SO2的漂白性、还原性和氧化性,实验室用品红溶液检验漂白性,碘具有氧化性,可以检验二氧化硫的还原性;硫化氢具有还原性,可以检验二氧化硫的氧化性;
所以B中盛放物质是品红溶液,碘和二氧化硫、水反应生成硫酸、HI,C中盛放物质是碘水,离子反应方程式为SO2+I2+2H2O═SO42-+2I-+4H+;
故答案为:品红溶液;SO2+I2+2H2O═SO42-+2I-+4H+;
(2)比较两个装置知,A2装置优点为:①不用加热,安全性能高.②易于控制反应进行,反应更充分,
故答案为:①不用加热,安全性能高.②易于控制反应进行,反应更充分.
点评 本题考查二氧化硫性质及检验、实验装置评价等知识点,为高频考点,二氧化硫具有漂白性、氧化性和还原性,根据试剂性质确定检验目的,注意二氧化硫和碘发生的反应,题目难度不大.


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:解答题
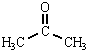 +CH3COOH
+CH3COOH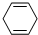
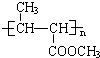 有一种合成这种高聚物的途径副产物污染少或无污染,原子利用率较高,符合“绿色化学挑战计划”的要求,其合成路线如下:
有一种合成这种高聚物的途径副产物污染少或无污染,原子利用率较高,符合“绿色化学挑战计划”的要求,其合成路线如下: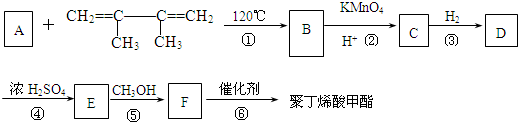
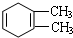 C:
C: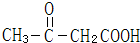
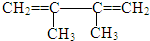 的系统命名名称是2,3-二甲基-1,3-丁二烯,反应⑥属于加聚反应(填反应类型)
的系统命名名称是2,3-二甲基-1,3-丁二烯,反应⑥属于加聚反应(填反应类型)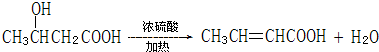 反应⑤:
反应⑤:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.4mol | B. | 0.3 mol | C. | 0.2mol | D. | 0.1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
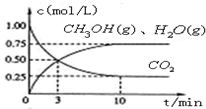
| 化学式 | 颜色 | Ksp |
| AgCl | 白色 | 2.0×10-10 |
| AgBr | 浅黄色 | 5.4×10-13 |
| AgI | 黄色 | 8.3×10-17 |
| Ag2S | 黑色 | 2.0×10-48 |
| Ag2CrO4 | 红色 | 2.0×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,E原子的价电子排布式为3s23p5,F在周期表中的位置是第四周期第IVB族.
,E原子的价电子排布式为3s23p5,F在周期表中的位置是第四周期第IVB族.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com