
(1)已知某反应的平衡常数表达式为:K=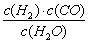 ,则它所对应反应的化学方程式是 ▲ 。
,则它所对应反应的化学方程式是 ▲ 。
(2) 合成甲醇的主要反应是:2H2(g)+CO(g) CH3OH(g) △H=-90.8 kJ·mol-1,t℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应l0min后测得各组分的浓度如下:
CH3OH(g) △H=-90.8 kJ·mol-1,t℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应l0min后测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度(mol/L) | 0.2 | 0.1 | 0.4 |
(A)该时间段内反应速率v(H2)= ▲
(B)比较此时正、逆反应速率的大小:v正 ▲ v逆(填“>”、“<”或“=”)
(C)反应达到平衡后,保持其它条件不变,若只把容器的体积缩小一半,平衡向 ▲
(填“逆向”、“正向”或“不”)移动,平衡常数K ▲ (填“增大”、“减小” 或“不变”)。
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案科目:高中化学 来源: 题型:
下列反应不属于氧化还原反应的是 ( )
A. 2H2O2 = 2H2O + O2↑; B.CuCl2+2NaOH==Cu(OH)2↓+2NaCl
C.2Na+2H2O=2NaOH+H2↑ D.3CO+Fe2O3 ==2Fe+3CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于浓硫酸和浓硝酸的叙述不正确的是( )
A.加热条件下均能与碳反应 B.长期露置在空气中浓度均会降低
C.常温下均不能用铁制容器贮存 D.一定条件下均可与铜片反应
查看答案和解析>>
科目:高中化学 来源: 题型:
 而与具体反应进行的途径无关。物质A在一定条件下可发生一系列转化,由右图判断下列
而与具体反应进行的途径无关。物质A在一定条件下可发生一系列转化,由右图判断下列
关系错误的是
A.A→F,△H = - △H 6
B.△H1+△H 2+△H 3+△H 4+△H 5+△H 6=1
C.C→F,|△H| = |△H 1+△H 2+△H 6 |
D.△H 1+△H 2+△H 3 = -△H 4-△H5-△H 6
查看答案和解析>>
科目:高中化学 来源: 题型:
碘与氢气反应的热化学方程式为:
①I2(g)+H2(g) 2HI(g) ΔH= - 9.48 kJ·mol-1
2HI(g) ΔH= - 9.48 kJ·mol-1
②I2(s)+H2(g) 2HI(g) ΔH= + 26.48 kJ·mol-1,由此判断下列说法或反应正确的是
2HI(g) ΔH= + 26.48 kJ·mol-1,由此判断下列说法或反应正确的是
A.反应①的产物比反应②的产物稳定
B.I2(s) I2(g) ΔH= + 17.00 kJ·mol-1
I2(g) ΔH= + 17.00 kJ·mol-1
C.反应②的反应物总能量比反应①的反应物总能量低
D.1 mol I2(g)中通入1 mol H2(g),反应后放热9.48 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
世界卫生组织(WHO)将ClO2列为A1级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒方面有广泛的应用。ClO2属于
A. 酸 B. 碱 C. 氯化物 D.氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作正确的是
A.过滤时为加快速度,可先将上层清液注入过滤器中,再将沉淀转移到过滤器中
B.蒸发时用玻璃棒搅拌,是为了使析出的固体重新溶解
C.蒸馏时需从冷凝管上口进水,下口出水
D.分液时,下层液体放完后,再从下口放出上层液体
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.有以下几种物质:①食盐晶体 ②乙醇 ③水银 ④蔗糖 ⑤冰醋酸(纯醋酸晶体)
⑥KNO3溶液 ⑦熔融的氢氧化钠 ⑧液态氯化氢 填空回答(填序号):
(1)物质中构成的微粒只能在固定位置上振动的是 ;(2)以上物质可以导电是 ;
(3)以上物质中属于电解质的是 ; (4)以上物质中属于非电解质是 。
Ⅱ. (1) O2、SO2、SO3三者质量之比为1∶2∶5,则它们的氧原子数之比为 。
(2)某金属氯化物MCl2 40.5 g中含有0.6 mol Cl-,则MCl2的摩尔质量为 ,金属M的相对原子质量为 。
(3)在V LFe2(SO4)3溶液中含有m g Fe3+,则C Fe3+为_______________;从中取出V/4L溶液,则SO42-物质的量浓度为_______________;再将这V/4L溶液溶液稀释到4L,稀释后溶液中溶质的物质的量浓度为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列叙述正确的是
A.lmol FeI2与足量氯气反应时转移的电子数为2NA
B.2 L0.5 mol • L-1硫酸钾溶液中阴离子所带电 荷数为NA
荷数为NA
C.1 mo l Na2O2固体中含离子总数为4NA
l Na2O2固体中含离子总数为4NA
D.丙烯和环丙烷组成的42 g混合气体 中氢原子的个数为6 NA
中氢原子的个数为6 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com