

分析 A是面粉中的主要成分,则A为淀粉,化学式为:(C6H10O5)n;A充分水解得B,B发酵得C、C氧化生成D,D能与新制的Cu(OH)2反应产生砖红色沉淀,则D中含有醛基,所以B为葡萄糖:CH2OH(CHOH)4CHO,葡萄糖发酵生成乙醇,则C为乙醇,乙醇氧化生成乙醛,则D为乙醛,乙醛氧化生成乙酸,则E为乙酸,符合B与E的实验式相同的条件,乙酸与乙醇发生正反应生成F,则F为乙酸乙酯,据此进行解答.
解答 解:A是面粉中的主要成分,则A为淀粉,化学式为:(C6H10O5)n;A充分水解得B发酵得C、C氧化生成D,D能与新制的Cu(OH)2反应产生砖红色沉淀,则D中含有醛基,所以B为葡萄糖:CH2OH(CHOH)4CHO,葡萄糖发酵生成乙醇,则C为乙醇,乙醇氧化生成乙醛,则D为乙醛,乙醛氧化生成乙酸,则E为乙酸,符合B与E的实验式相同的条件,乙酸与乙醇发生正反应生成F,则F为乙酸乙酯,
(1)根据分析可知,A为淀粉,化学式为:(C6H10O5)n;B为葡萄糖,结构简式为:CH2OH(CHOH)4CHO,与葡萄糖互为同分异构体的一种物质为果糖,
故答案为:(C6H10O5)n;CH2OH(CHOH)4CHO;果糖;
(2)F为乙酸乙酯,乙酸乙酯在稀硫酸中发生水解反应生成乙酸和乙醇,反应的化学方程式为:CH3COOCH2CH3+H2O$→_{△}^{稀硫酸}$CH3COOH+CH3CH2OH,
故答案为:CH3COOCH2CH3+H2O$→_{△}^{稀硫酸}$CH3COOH+CH3CH2OH;
(3)E为乙酸,乙酸与氨水发生的离子方程式为CH3COOH+NH3.H2O=CH3COO-+NH4++H2O,乙酸与碳酸氢钠反应生成乙酸钠、二氧化碳气体和水,反应的化学方程式为:CH3COOH+NaHCO3=CH3COONa+H2O+CO2↑,
故答案为:CH3COOH+NH3.H2O=CH3COO-+NH4++H2O;CH3COOH+NaHCO3=CH3COONa+H2O+CO2↑;
(4)能够与新制Cu(OH)2反应产生砖红色沉淀的物质中一定含有醛基,A到F中含有醛基的为葡萄糖和乙醛,
故答案为:葡萄糖和乙醛;
(5)C为乙醇,钠与C的反应方程式为2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,
故答案为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;
(6)C→D的反应方程式为2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O;
(7)C+E→F的反应方程式为C2H5OH+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O,
故答案为:C2H5OH+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O.
点评 本题为有机推断,侧重考查了常见有机物结构与性质,题目难度中等,熟练掌握常见有机物结构与性质为解答关键,要求学生能够正确书写常见有机反应方程式,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
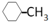 +H2
+H2
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象及相关结论 |
| ①取少量电解质溶液于试管中,用pH试纸测其pH. | →试纸呈深蓝色,经比对溶液的pH约为14,说明溶液中有残余的KOH. |
| ②继续加入足量1mol•L-1HCl 溶液,再加入少量0.1mol•L-1BaCl2溶液,振荡. | →若有白色沉淀产生,则溶液中含有K2SO4. →若无白色沉淀产生,则溶液中没有K2SO4. |
| ③另取少量电解质溶液于试管中,先加1mol•L-1的H2SO4酸化,再滴入2~3滴0.01mol•L-1KMnO4酸性溶液,振荡. | →若KMnO4溶液紫红色褪去,则说明溶液中含有K2SO3,若KMnO4溶液紫红色不褪,则说明溶液不含K2SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度不相同 | |
| B. | 由于Ksp(BaSO4)<Ksp(BaCO3),因此不可能使BaSO4沉淀转化为BaCO3沉淀 | |
| C. | 常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 | |
| D. | 含1mol[Co(NH3)5Cl]Cl2的溶液与足量的AgNO3溶液混合,能生成2mol的AgCl沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

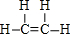 ;B的结构简式:CH3CH3;
;B的结构简式:CH3CH3;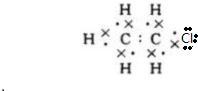 ;D的官能团名称羟基;G官能团的结构简式-COOH.
;D的官能团名称羟基;G官能团的结构简式-COOH.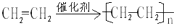 (反应类型加聚反应).
(反应类型加聚反应).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内消耗2n molSO2的同时生成2n molS03,说明该反应达到平衡状态 | |
| B. | 达到化学平衡时,SO2、02和SO3的物质的量浓度均保持不变 | |
| C. | 达到化学平衡时,正反应和逆反应的速率都为零 | |
| D. | 达到化学平衡时,SO2将完全转化为SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④② | B. | ②④①②③ | C. | ④②③①② | D. | ②④②③① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com