

���� ��1������NaOH��Һ��SO2��Ӧ��������������ˮ��
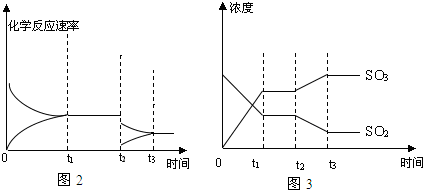
��2�����SO2ƽ��ת���ʣ��ٽ���ѧƽ�������ƶ������ݻ�ѧƽ���ƶ�Ӱ�������жϣ�
��3����ߴ���Ч�ʿ���ͨ���������塢�����¶���400��500�桢��������뷴Ӧ����ĽӴ������
��4�����ݻ�ѧƽ��״̬�����жϣ����ݡ�����ʽ�������м���ó����ۣ�
��5��������������Ի�ѧƽ���Ӱ���жϣ�
��� �⣺��1������NaOH��Һ��SO2��Ӧ��������������ˮ�����ӷ���ʽΪSO2+2OH-=SO32-+H2O���ʴ�Ϊ��SO2+2OH-=SO32-+H2O��
��2�����SO2ƽ��ת���ʣ��ٽ���ѧƽ�������ƶ���
A������Ӧ�������������С����Сѹǿ����ѧƽ�����淴Ӧ�����ƶ�����A����
B������Ӧ������ȣ������¶ȣ���ѧƽ�����淴Ӧ�����ƶ�����B����
C����������Ũ�ȣ���ѧƽ�������ƶ�����C��ȷ��
D����С������Ũ�ȣ���ѧƽ�������ƶ�����D��ȷ��
�ʴ�Ϊ��CD��
��3����ߴ���Ч�ʿ���ͨ���������塢�����¶���400��500�桢��������뷴Ӧ����ĽӴ������
�ʴ�Ϊ���������塢�����¶���400��500�棻��������뷴Ӧ����ĽӴ�����ȣ�
��4����A����Ӧ���������ȫ�����壬�����������䣬����������䣬��������ܶ�ʼ�ղ��䣬�����ܶȲ��䲻��˵����Ӧ�ﵽƽ��״̬����Aѡ��
B��SO2�ٷֺ������ֲ��䣬��������Ũ�Ȳ��ٷ����仯���ﵽ��ѧƽ��״̬����B��ѡ��
C����Ӧǰ���������ʵ�����ͬ�������������ѹǿ���䣬��ﵽ��ѧƽ��״̬����C��ѡ��
D��SO3������������SO2������������ȣ���Ϊ����Ӧ�������ж����淴Ӧ�����Ƿ���ȣ������ж��Ƿ�ƽ�⣬��Dѡ��
E����Ӧǰ���������ʵ�����ͬ����������������ʵ������䣬��ﵽ��ѧƽ��״̬����E��ѡ��
�ʴ�Ϊ��AD��
�ڸ������⣺2SO2��g��+O2��g��?2SO3��g����
��ʼ���ʵ�����2 1 0
�仯���ʵ�����2x x 2x
ƽ�����ʵ�����2-2x 1-x 2x
��ƽ�ⳣ��ΪK=$\frac{[S{O}_{3}]^{2}}{[S{O}_{2}]^{2}•[{O}_{2}]}$=$\frac{��\frac{2x}{2}��^{2}}{��\frac{2-2x}{2}��^{2}����\frac{1-x}{2}��}$=$\frac{2{x}^{2}}{��1-x��^{3}}$��
�ʴ�Ϊ��$\frac{2{x}^{2}}{��1-x��^{3}}$��
��5��ͼ2��ʱ��t2SO3Ũ������SO2Ũ�ȼ�С������ѧƽ�������ƶ�����������t2ʱ������Ũ�Ȳ��䣬��ѹǿ���䣬����˵��������Ϊѹǿ�仯������ƽ����ƶ���ֻ��Ϊ�¶ȵ�Ӱ�죬��������Ϊ�����¶ȣ��ʴ�Ϊ�������¶ȣ�
���� ������һ���ۺ��ԵĿ��⣬�漰��ѧ��Ӧ���ʡ���ѧƽ�ⳣ������ѧƽ����ƶ��Լ�v-tͼ��֪ʶ���ѶȽϴ��ۺ���ǿ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ��ϩ | C�� | ���� | D�� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.05mol/��L•s�� | B�� | 0.05mol/L | C�� | 0.20 mol/��L•s�� | D�� | 0.20mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D | |
| ǿ����� | HCl | �ƾ� | CH3COOH | NaCl |
| ������� | NH3•H2O | HClO | BaSO4 | NaOH |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
 ��2L�ĺ����ܱ������У�������Ӧ��A��g��+B��g��?2C��g��+D��s����H=-a kJ•mol-1��ʵ�����ݺͽ���ֱ��������ͼ��ʾ������˵����ȷ���ǣ�������
��2L�ĺ����ܱ������У�������Ӧ��A��g��+B��g��?2C��g��+D��s����H=-a kJ•mol-1��ʵ�����ݺͽ���ֱ��������ͼ��ʾ������˵����ȷ���ǣ�������| ʵ�� ��� | �¶� | ��ʼ���ʵ��� | ���� �仯 | |
| A | B | |||
| �� | 600�� | 1 mol | 3 mol | 96 kJ |
| �� | 800�� | 0.5 mol | 1.5mol | -- |
| A�� | ʵ����У�10 min��ƽ������v��B��=0.06 mol•L-1•min-1 | |
| B�� | 600��ʱ����������ʽ��a=160 | |
| C�� | 600��ʱ���÷�Ӧ��ƽ�ⳣ����0.45 | |
| D�� | ��ʵ����ƽ����ϵ���ٳ���0.5 mol A��1.5 mol B��A��ת���ʲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ϊ���ȷ�Ӧ | |
| B�� | Ϊ���ȷ�Ӧ | |
| C�� | ��Ӧ����������ת��Ϊ��ѧ�� | |
| D�� | ��Ӧ�������������������������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com