
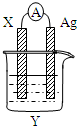
 依据氧化还原反应2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.回答下列问题.
依据氧化还原反应2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.回答下列问题.分析 根据反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”分析,在反应中,Cu被氧化,失电子,应为原电池的负极,电极反应为Cu-2e-=Cu2+,则正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,电解质溶液为AgNO3 ,原电池中,电子从负极经外电路流向正极,根据得失电子数相等计算.
解答 解:根据电池反应式知,铜失电子作负极,结合图片可知,银作正极,
(1)铜作负极,银作正极,所以X是铜,银电极所在的电解质溶液为可溶性的银盐溶液,所以Y溶液是硝酸银溶液,
故答案为:铜;AgNO3溶液;
(2)正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,
故答案为:正极; Ag++e-=Ag;
(3)电子从负极铜沿导线流向银,
故答案为:铜;银;
(4)n(Cu)=$\frac{1.6g}{64g/mol}$=0.025mol,则失去0.05mol电子,由Ag++e-=Ag可知,生成0.05molAg,
则m(Ag)=0.05mol×108g/mol=5.4g,
故答案为:5.4g.
点评 本题考查了原电池,明确原电池原理即可解答,注意(3)中电子不进入电解质溶液,电解质溶液中阴阳离子的定性移动而构成闭合回路,为易错点.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
 在盛有溴水的三支试管中分别加入少量苯、四氯化碳和酒精,振荡后静置,出现下列现象,正确的结论是( )
在盛有溴水的三支试管中分别加入少量苯、四氯化碳和酒精,振荡后静置,出现下列现象,正确的结论是( )| A. | ①加CCl4 ②加苯 ③加酒精 | B. | ①加酒精 ②加CCl4 ③加苯 | ||
| C. | ①加苯 ②加CCl4 ③加酒精 | D. | ①加苯 ②加酒精 ③加CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2•8H2O晶体和NH4Cl混合搅拌 | B. | 硫酸与氢氧化钠反应 | ||
| C. | 锌和盐酸反应 | D. | 氢气和氧气的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
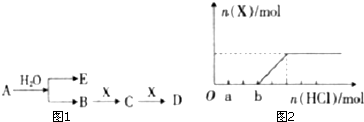
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
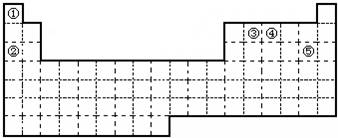
 ,试比较②和③原子半径的大小②>③(填“>”或“<”)
,试比较②和③原子半径的大小②>③(填“>”或“<”)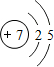 ,该元素的最高价氧化物的水化物能与Cu发生反应,反应中作氧化剂的是(写化学式)HNO3.
,该元素的最高价氧化物的水化物能与Cu发生反应,反应中作氧化剂的是(写化学式)HNO3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有物质中都存在化学键 | |
| B. | 由两种元素组成的分子中一定不存在非极性共价键 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 化学键断裂的过程必发生化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
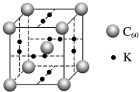 科学家把C60和K掺杂在一起制造出的化合物具有超导性能,其晶胞如图所示.该化合物中的K原子和C60分子的个数比为( )
科学家把C60和K掺杂在一起制造出的化合物具有超导性能,其晶胞如图所示.该化合物中的K原子和C60分子的个数比为( )| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑥ | B. | ①②③④⑥ | C. | ①②③⑥ | D. | ①②③④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用适当的催化剂只改变正反应速率 | |
| B. | 降低压强能提高逆反应速率 | |
| C. | 升高温度能同时提高正、逆反应速率 | |
| D. | 减小压强对正反应速率影响小于逆反应速率的影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com