
| 官能团 | 选择试剂 | 实验现象 | 有关反应的化学方程式或离子方程式 |
分析 有机物含有羟基,可与钠反应生成氢气,含有醛基,具有还原性,可发生银镜反应,在加热条件下,可与新制备氢氧化铜浊液发生氧化还原反应,以此解答该题.
解答 解:含有醛基,具有还原性,可发生银镜反应,方程式为HOCH2CH2CHO+2[Ag(NH3)2]++2OH-→HOCH2CH2COO-+2Ag↓+NH4++H2O+3NH3,在加热条件下,可与新制备氢氧化铜浊液发生氧化还原反应,方程式为HOCH2CH2CHO+2 Cu(OH)2→HOCH2CH2COOH+Cu2O↓+2H2O,
含有羟基,可与钠反应生成氢气,方程式为2 HOCH2CH2CHO+2Na→2 NaOCH2CH2CHO+H2↑,
故答案为:
1 | -CHO | 新制氢氧化铜 | 开始无变化,加热后出现砖红色沉淀 | HOCH2CH2CHO+2 Cu(OH)2→ HOCH2CH2COOH+Cu2O↓+2H2O |
| 2 | -CHO | 银氨溶液 | 水浴加热后出现银镜 | HOCH2CH2CHO+2[Ag(NH3)2]++2OH-→HOCH2CH2COO-+2Ag↓+NH4++H2O+3NH3 |
| 3 | -OH | 钠 | 有气泡产生 | 2 HOCH2CH2CHO+2Na→2 NaOCH2CH2CHO+H2↑ |
点评 本题涉及有机物的结构和性质方面的知识,注意有机物的结构决定性质,根据官能团来判断有机物的性质并书写方程式即可,难度不大.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

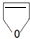 或
或 .
.


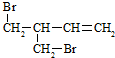
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
 ;Ca的最外层电子数为2.
;Ca的最外层电子数为2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 二氧化氯消毒液1000mL | |
| 溶质的质量分数 | 80% |
| 密度 | 1.2g/cm3 |
| 强腐蚀性,阴冷,密封储存 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱性锌锰电池是二次电池 | |
| B. | 铅蓄电池是二次电池 | |
| C. | 二次电池又叫蓄电池,它放电后可以再充电使活性物质获得再生 | |
| D. | 燃料电池的活性物质没有储存在电池内部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
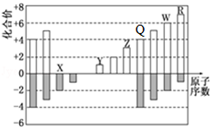
| A. | 原子半径:Z>Y>X | |
| B. | X和Z形成的化合物能溶于NaOH溶液 | |
| C. | Q和X形成的化合物不能与酸反应 | |
| D. | R元素的含氧酸和W元素的含氧酸,酸性一定前者强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
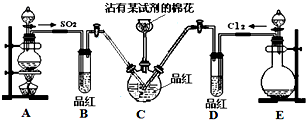 探究SO2和氯水的漂白性,设计了如下实验,装置如图.
探究SO2和氯水的漂白性,设计了如下实验,装置如图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com