
下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最活泼的非金属原子的原子结构示意图为 。
(2)地壳中含量最多的金属元素是 (写元素符号) 。
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 。
(4)写出⑤与氢氧化钠反应的化学方程式: ,
写出⑤的氢氧化物与氢氧化钠溶液完全反应的离子方程式:
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源:2016届湖北省高三上学期12月月考理综化学试卷(解析版) 题型:选择题
对下列装置图的叙述正确的是
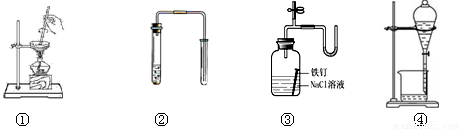
A.装置①可用于加热蒸干氯化铵溶液得到氯化铵晶体
B.装置②可用于铜和稀硝酸制取并收集少量NO
C.装置③可用于证明铁生锈氧气参与反应
D.苯萃取碘水中的碘后,从装置④下口放出的是碘的苯溶液
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省分校高三上学期12月月考理综化学试卷(解析版) 题型:选择题
26g锌和含63gHNO3的稀硝酸正好完全反应,生成的还原产物的相对分子质量可能是( )
A. 80 B. 30 C. 46 D. 28
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西柳州铁路第一中学高二上段考理化学卷(解析版) 题型:填空题
I.(1)H3PO2是一元中强酸,写出其电离方程式_________________________________。
(2)③NaH2PO2为________(填“正盐”或“酸式盐”),其溶液显______(填“酸性”、“中性”或“碱性”)。
II.现有pH=2的醋酸甲和pH=2的盐酸乙:
(1)取10 mL的甲溶液,加入等体积的水,醋酸的电离平衡________(填“向左”、“向右”或“不”)移动;若加入少量的冰醋酸,醋酸的电离平衡________(填“向左”、“向右”或“不”)移动,若加入少量无水醋酸钠固体,待固体溶解后,溶液中c(H+)/c(CH3COOH)的值将________(填“增大”、“减小”或“无法确定”)。
(2)相同条件下,取等体积的甲、乙两溶液混合,溶液的pH=___ ___,若两溶液不等体积混合,则
pH___ ___。
(3)各取25 mL的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和至pH=7,则消耗的NaOH溶液的体积大小关系为V(甲)________ V(乙) ( 填“>”、“<”或“=”)。
(4)取25 mL的甲溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+)、c(CH3COO-)的大小关系为c(Na+)________ c(CH3COO-) ( 填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省嘉兴、杭州、宁波五校高三上第一次联考化学试卷(解析版) 题型:选择题
微生物燃料电池(Microbial Fuel Cell,MFC)是一种利用微生物将有机物中的化学能直接转化成电能的装置。最早用于有机废水处理,下图是利用微生物燃料电池处理含甲醛废水的装置,其中3是质子交换膜,下列有关说法不正确的是
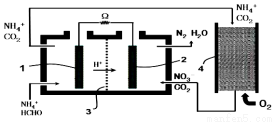
A.负极发生的反应为:HCHO-4e-+H2O=CO2+4H+
B.负极所在的左室中需保持厌氧环境
C.O2参与正极反应,发生还原反应
D.NH4+通过循环操作最终被转化成N2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西桂林中学高二上期中考试理化学试卷(解析版) 题型:选择题
下列有关说法不正确的是
A.纤维素、油脂、蛋白质均为高分子化合物
B.35%~40%的甲醛水溶液称为福尔马林,具有杀菌、防腐性能
C.淀粉、溴乙烷、脂肪在一定条件下都可以发生水解反应
D.脂肪烃的来源有石油、天然气和煤等,通过石油的裂化及裂解可得到气态烯烃
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高一上期中考试化学试卷(解析版) 题型:选择题
下列实验或事故处理的方法中,不正确的是
A.完 成用CCl4萃取碘水后的实验后,溶液要回收
成用CCl4萃取碘水后的实验后,溶液要回收
B.不慎将浓碱沾到皮肤上,应立即用大量水冲洗,然后涂上硼酸溶液
C.如果汽油、煤油等可燃物着火,应立即用水扑灭
D.酒精灯不慎碰翻着火,应立即用湿布盖灭
查看答案和解析>>
科目:高中化学 来源:2016届福建省三明市高三上学期第二次月考化学试卷(解析版) 题型:填空题
以含钴废催化剂(主要成分为Co、Fe、SiO2)为原料,制取钴的氧化物的流程如下:
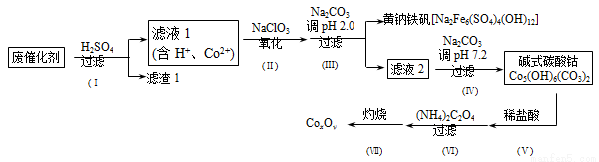
(1)步骤Ⅰ中废催化剂用硫酸浸出后,将滤渣1进行再次浸出,其目的是____________。
(2)步骤Ⅱ需要加热搅拌,相应的离子方程式为_____________________。
(3)步骤Ⅲ中的反应为2Na++6Fe3++4SO42-+12H2O=Na2Fe6(SO4)4(OH)12+12H +。过滤后母液的pH = 2.0,c(Na+) =a mol·L-1,c(Fe3+) =b mol· L-1,c(S
L-1,c(S O42-)= d mol·L-1,该反应的平衡常数K=___(用含a 、b 、d 的代数式表示)。
O42-)= d mol·L-1,该反应的平衡常数K=___(用含a 、b 、d 的代数式表示)。
(4)完成步骤Ⅳ中反应的离子方程式:
□_______+□CO32-+□H2O=Co5(OH)6(CO3)2↓+□_____
(5)已知CoCl2的溶解度曲线如图所示。步骤Ⅴ向碱式碳酸钴中加入足量稀盐酸,边加热边搅拌,待固体溶解后需趁热过滤。
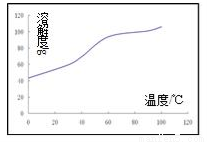
①边加热边搅拌的原因是______________;
②趁热过滤的原因是_______ _______。
_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com