
【题目】治理SO2、CO、NOx污染是化学工作者研究的重要课题。
Ⅰ.硫酸厂大量排放含SO2的尾气会对环境造成严重危害。
(1)工业上可利用废碱液(主要成分为Na2CO3)处理硫酸厂尾气中的SO2,得到Na2SO3溶液,该反应的离子方程式为__________________________________。
Ⅱ.沥青混凝土可作为反应;2CO(g)+O2(g)![]() 2CO2(g)的催化剂。图甲表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
2CO2(g)的催化剂。图甲表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。

(2)a、b、c、d 四点中,达到平衡状态的是__________________________________。
(3)已知c点时容器中O2浓度为0.02 mol/L,则50℃时,在α型沥青混凝土中CO转化反应的平衡常数K=____________(用含x的代数式表示)。
(4)下列关于图甲的说法正确的是_____________。
A.CO转化反应的平衡常数K(a)
B.在均未达到平衡状态时,同温下β型沥青混凝土中CO转化速率比α型要大
C.b点时CO与O2分子之间发生有效碰撞的几率在整个实验过程中最高
D.e点转化率出现突变的原因可能是温度升高后催化剂失去活性
Ⅲ.某含钴催化剂可以催化消除柴油车尾气中的碳烟(C)和NOx。不同温度下,将模拟尾气(成分如下表所示)以相同的流速通过该催化剂,测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图乙所示。
模拟尾气 | 气体(10mol) | 碳烟 | ||
NO | O2 | He | ||
物质的量(mol) | 0.025 | 0.5 | 9.475 | n |
(5)375℃时,测得排出的气体中含0.45 molO2和0.0525 mol CO2,则Y的化学式为______________。

(6)实验过程中采用NO模拟NOx,而不采用NO2的原因是____________________________。
【答案】 CO32-+SO2=SO32-+CO2 bcd 50x2/(1-x)2 BD N2O 由于存在反应2NO2![]() N2O4会导致一定的分析误差
N2O4会导致一定的分析误差
【解析】(1)利用强酸制备弱酸规律,亚硫酸的酸性强于碳酸,因此碳酸钠溶液与二氧化硫反应生成亚硫酸钠和二氧化碳,离子方程式为CO32-+SO2=SO32-+CO2;正确答案:CO32-+SO2=SO32-+CO2。
(2)可逆反应达到平衡状态时,转化率为最大转化率,因此使用同质量的不同沥青混凝土(α型、β型)催化时,b、c对应的转化率最大,反应达到平衡状态,达到平衡状态后,再升高温度,平衡左移,一氧化碳的转化率减小,所以d点也为对应温度下的平衡状态;正确答案:bcd。
(3)假设一氧化碳的起始浓度为a,其转化率为x;
2CO(g)+O2(g)![]() 2CO2(g)
2CO2(g)
起始浓度 a 0
变化浓度 ax ax
平衡浓度 a-ax 0.02 ax
平衡常数K=c2(CO2)/c2(CO)c(O2)=(ax)2/[(a-ax)2×0.02]=50x2/(1-x)2 ;正确答案:50x2/(1-x)2。
(4)平衡常数为温度的函数,a、c处在同一温度下,所以K(a)=K(c),A错误;从图像可以看出,同温下β型沥青混凝土催化下,催化能力强于α型,所以在均未达到平衡状态时,同温下β型沥青混凝土中CO转化速率比α型要大,B正确;反应物的浓度越大,分子之间发生有效碰撞的几率越高,b点时达到平衡时的点,一氧化碳的转化率最大,剩余物质的浓度最小,有效碰撞几率不是最高的,C错误;温度太高,催化剂可能会失去活性,催化能力下降,D正确;正确选项BD。
(5)模拟尾气中一氧化氮的物质的量为 0.025 mol,而图中参与反应生成X和Y的一氧化氮的物质的量为:![]() ,模拟尾气中
,模拟尾气中![]() 的物质的量为0.5 mol,测得排出的气体中含
的物质的量为0.5 mol,测得排出的气体中含![]() ,说明实际参与反应的氧气的物质的量为
,说明实际参与反应的氧气的物质的量为![]() ,同时测得
,同时测得![]() ,根据氧守恒,可以知道一氧化二氮的物质的量为:
,根据氧守恒,可以知道一氧化二氮的物质的量为:![]() ,根据氮守恒可以知道氮气的物质的量为:
,根据氮守恒可以知道氮气的物质的量为:![]() ,所以
,所以![]() 对应的是氮气,而8%对应是一氧化二氮,即Y对应是
对应的是氮气,而8%对应是一氧化二氮,即Y对应是![]() ;正确答案:
;正确答案:![]() 。
。
(6)实验过程中采用NO模拟NOx,而不采用NO2的原因是二氧化氮与四氧化二氮之间存在双聚平衡,所以无纯的二氧化氮;正确答案:由于存在反应2NO2![]() N2O4会导致一定的分析误差。
N2O4会导致一定的分析误差。


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案科目:高中化学 来源: 题型:
【题目】香烟烟雾中往往含有CO和SO2气体,下列关于这两种气体的说法正确的是( )
A.两者都易溶于水
B.两者都污染环境,危害健康
C.两者都能使品红溶液褪色
D.两者都是形成酸雨的主要原因
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验.
实验I:反应产物的定性探究
按如图装置(固定装置已略去)进行实验
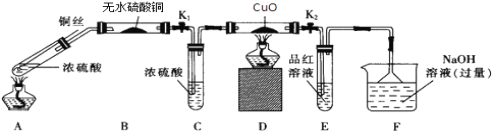
(1)A装置的试管中发生反应的化学方程式是____________;B装置的作用是________E装置中的现象是_______;
(2)实验过程中,能证明无氢气生成的现象是________。
(3)F装置的烧杯中发生反应的离子方程式是_____________________。
实验Ⅱ:反应产物的定量探究
(4)为测定硫酸铜的产率,将该反应所得溶液中和后配制成250.00 mL溶液,取该溶液25.00mL加入足量KI溶液中振荡,生成的I2恰好与20.00 mL 0.30 molL﹣1的Na2S2O3溶液反应,若反应消耗铜的质量为6.4g,则硫酸铜的产率为________。(已知2Cu2++4I﹣=2CuI+I2, 2S2O32﹣+I2=S4O62﹣+2I﹣)(注:硫酸铜的产率指的是硫酸铜的实际产量与理论产量的比值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是以实验为基础的.利用已学知识对下列实验进行分析并填空:
Ⅰ.某研究性学习小组设计了一组实验来探究元素周期律.
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置完成同主族元素C、Si非金属性强弱比较的实验研究;
乙同学设计了如图2装置实验来验证卤族元素性质的递变规律(夹持装置已略去).A、B、C三个胶头滴管分别是氯酸钾溶液、NaBr溶液、淀粉KI溶液.已知常温下浓盐酸与氯酸钾溶液能反应生成氯气.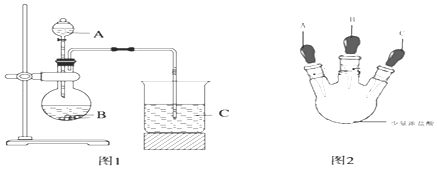
(1)甲同学设计实验所涉及的离子方程为:、 .
(2)乙同学具体操作如下:
①先挤压胶头滴管A,使少量溶液滴入烧瓶内;
②挤压胶头滴管B,使稍过量溶液滴入烧瓶内,充分反应.写出该操作中主要离子方程式为 .
③再挤压胶头滴管C,使少量溶液滴入烧瓶内,可观察到;
(3)根据甲乙同学的实验可得到的结论是:
(4)II.
实验 |
| ||
实验 |
|
|
|
实验 | 结论: | ||
反应 | |||
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种因素:①温度和压强、②所含微粒数、③微粒本身大小、④微粒间的距离,其中对气体物质体积有显著影响的是
A.②③④B.②④C.①②④D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油裂解气主要含有丙烯、1,3-丁二烯等不饱和烃,以它们为原料可合成CR橡胶和医药中间体G,,合成路线如下:

已知:①B、C、D 均能发生银镜反应;
②
(1)A的顺式异构体的结构简式为___________________。
(2)C中含氧官能团的名称是____________,反应①的反应类型为____________________。
(3)写出E→ 反应的化学方程式:_________________________________。
(4)写出同时满足下列条件的医药中间体G的同分异构体的结构简式: __________________。
①与D 互为同系物; ②核磁共振氢谱有三组峰。
(5)用简要语言表述检验B中所含官能团的实验方法:_______________________。
(6)以A为起始原料合成CR橡胶的线路为______________________(其它试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 大米富含淀粉
B. 加碘食盐含有碘酸钾(KIO3)
C. 人体必需的微量元素就是维生素
D. 人体必需的微量元素不都是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知空气﹣锌电池的电极反应为:锌片:Zn+20H﹣﹣2e﹣=ZnO+H20,石墨:02+2H20+4e﹣=40H﹣ . 根据此判断,锌片是( )
A.负极,并被氧化
B.负极,并被还原
C.正极,并被氧化
D.正极,并被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用膜技术原理和电化学原理制备少量硫酸和绿色硝化剂N2O5,装置如图所示,下列说法不正确的是

A. 电极a和电极c都发生氧化反应
B. 电极d的电极反应式为2H++2e-=H2↑
C. c电极上的电极反应式为N2O4-2e-+H2O=N2O5+2H+
D. 装置A中每消耗64gSO2,理论上装置A和装置B中均有2moH+通过质子交换膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com