
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中正确的是
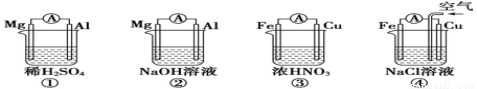
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为:2H2O+2e-= 2OH-+H2↑
C.③中Fe作负极,电极反应式为Fe-2e-= Fe2+
D.④中Cu作正极,电极反应式为2H++2e-= H2↑
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中理科化学试卷(解析版) 题型:选择题
根据元素周期表和元素周期律分析下面的推断,其中错误的是( )
A.铍(Be)的原子失电子能力比镁弱
B.砹(At)的氢化物不稳定
C.硒(Se)化氢比硫化氢稳定
D.氢氧化锶[Sr(OH)2]比氢氧化钙的碱性强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附中高一下期中化学试卷(解析版) 题型:选择题
银锌钮扣高能电池放电时的反应为:Zn+Ag2O==ZnO+2Ag,下列说法中不正确的是
A.若电解质溶液为KOH溶液,则电池工作一段时间后pH有明显变化
B.Zn作负极,被氧化
C.Ag2O在正极上发生还原反应
D.电解质溶液中的阴离子移向负极
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附中高一下期中化学试卷(解析版) 题型:选择题
下列物质不属于有机物的是
A.C2H4 B.C12H22O11 C.C60 D.HCOOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海师大附二中高一下期中化学试卷(解析版) 题型:填空题
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/LH2SO4溶液中,乙同学将电极放入6mol/LNaOH溶液中,如图:
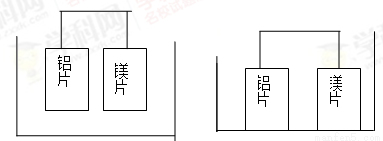
甲(H2SO4溶液) 乙(NaOH溶液)
(1)写出甲池中正极的电极反应式: ,负极的电极反应式: 。
(2)写出乙池中负极的电极反应式: ,乙池中总反应的离子方程式: 。
(3)如果甲和乙同学均认为,“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出 活动性更强,而乙会判断出 活动性更强。
(5)丙同学依据甲、乙同学的思路,设计如下实验:将铝片和铜片用导线相连.一组插入浓硝酸中,一组插入稀NaOH溶液中,分别形成了原电池。
①在这两个原电池中,负极分别为________。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
②写出插入浓硝酸中形成原电池的总反应化学方程式__________________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海师大附二中高一下期中化学试卷(解析版) 题型:选择题
已知1molH2(g)与1molBr2(l)完全反应生成2molHBr(g)放出72kJ的能量,方程式为:H2(g)+Br2(l)=2HBr(g);又知蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其它相关数据如下表:
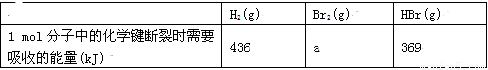
则表中a为
A.404 B.260 C.230 D.200
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海师大附二中高一下期中化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A.H2S、H2O、HF的热稳定性依次增强
B.相同条件下,H2S的沸点比H2O高
C.在过渡元素中寻找优良的催化剂
D.在周期表中金属元素与非金属元素交界处寻找半导体材料
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一下期中化学试卷(解析版) 题型:填空题
(1)请根据氧化还原反应Fe+2H+=Fe2++H2↑设计成原电池:
①负极材料为:__________发生的电极反应是: ,电流__________(填“流出”或“流入”)
②正极发生的电极反应是: ,该反应为 (填“氧化反应”或“还原反应”) 。
③若电路中转移6.02×1022个e﹣,则产生标况下H2的体积为_____ _____。
(2)铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中如图所示,则铁被腐蚀的速率由慢到快的顺序是(填序号) 。
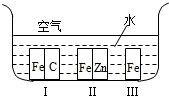
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下期中化学试卷(解析版) 题型:选择题
下列各组热化学方程式中,△H1>△H2的是
①C(s)+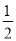 O2(g)=CO(g) △H1 C(s)+O2(g)=CO2(g) △H2
O2(g)=CO(g) △H1 C(s)+O2(g)=CO2(g) △H2
②S(s)+O2(g)=SO2(g) △H1 S(g)+O2(g)=SO2(g) △H2
③H2(g)+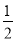 O2(g)=H2O(l) △H1 2H2(g)+O2(g)=2H2O(l) △H2
O2(g)=H2O(l) △H1 2H2(g)+O2(g)=2H2O(l) △H2
④CaCO3(s)===CaO(s)+CO2(g) △H1 CaO(s)+CO2(g)=== CaCO3(s) △H2
A.①③④ B.②③④ C.①②③④ D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com