

·ÖĪö Ā±“śĢžŌŚ¼īŠŌĢõ¼žĻĀĖ®½āÉś³É“¼£¬·“Ó¦ĶźČ«ŗó¼ÓČė¹żĮæĻõĖį£¬ŌŁ¼ÓČėĻõĖįŅųČÜŅŗÉś³ÉĀ±»ÆŅų³Įµķ£¬
£Ø1£©×¼Č·ĮæČ”11.40mLŅŗĢ壬ŠčŅŖÓĆ¾«ĆÜĮæ¾ß£¬¾«Č·µ½0.1£¬¹Ą¶Įµ½0.01£¬æÉÓƵĪ¶Ø¹Ü”¢ŅĘŅŗ¹ÜµČŅĒĘ÷£»
£Ø2£©¼ÓČėĻ”ĻõĖį£¬æɱÜĆāÉś³ÉAgOHµČ³Įµķ£»
£Ø3£©Éś³Éµ»ĘÉ«³Įµķ£¬ĖµĆ÷Éś³ÉAgBr£»
£Ø4£©øł¾Żn=$\frac{m}{M}$¼ĘĖćAgBrµÄĪļÖŹµÄĮ棬øĆĀ±“śĢžÕōĘų¶Ō¼×ĶéµÄĻą¶ŌĆܶȏĒ11.75£¬Ēó³öĘäĻą¶Ō·Ö×ÓÖŹĮ棬øł¾Żm=¦ŃV¼ĘĖćøĆÓŠ»śĪļµÄÖŹĮ棬ŌŁøł¾Żn=$\frac{m}{M}$Ēó³öĀ±“śĢžµÄĪļÖŹµÄĮæ£¬Č·¶ØĀ±“śĢžÖŠµÄĀ±Ō×ÓŹżÄæ£¬Č»ŗóČ·¶Ø·Ö×ÓŹ½£»øł¾ŻBrµÄŌ×ÓĮæŗĶĀ±“śĢžµÄĻą¶Ō·Ö×ÓÖŹĮæĒó³öĀ±“śĢžÖŠĢž»łµÄŹ½Į棬Ģž»łµÄŹ½Įæ³żŅŌ12£¬ÉĢĪŖĢ¼Ō×ÓŹż£¬ÓąŹżĪŖĒāŌ×ÓŹż£¬¾Ż“ĖŠ“³ö·Ö×ÓŹ½ŗĶ½į¹¹¼ņŹ½£®
½ā“š ½ā£ŗ£Ø1£©¼īŹ½µĪ¶Ø¹ÜµÄĻĀ¶ĖÓŠŅ»¶ĪĻšĘ¤¹Ü£¬Ā±“śĢžÓŠøÆŹ“ŠŌ£¬ĮæČ”Ā±“śĢžŅŖÓĆĖįŹ½µĪ¶Ø¹Ü»ņŅĘŅŗ¹Ü£¬¹Ź“š°øĪŖ£ŗĖįŹ½µĪ¶Ø¹Ü»ņŅĘŅŗ¹Ü£»
£Ø2£©ČÜŅŗÖŠŗ¬ÓŠ¼ī£¬¶ŌĀ±Ąė×ӵIJā¶ØÓŠÓ°Ļģ£¬ĖłŅŌ¹żĮæĻõĖįµÄ×÷ÓĆÖŠŗĶĒāŃõ»ÆÄĘ£¬¹Ź“š°øĪŖ£ŗÖŠŗĶĒāŃõ»ÆÄĘ£»
£Ø3£©Éś³ÉµÄ³ĮµķĪŖµ»ĘÉ«£¬ŌņøĆ³ĮµķĪŖAgBr£¬ĖłŅŌøĆĀ±“śĢžÖŠµÄĀ±Ō×ÓŹĒBr£¬¹Ź“š°øĪŖ£ŗBr£»
£Ø4£©³ĘµĆ³ĮµķµÄÖŹĮæĪŖ37.6g£¬n£ØAgBr£©=$\frac{m}{M}$=$\frac{37.6g}{188g/mol}$=0.2mol£¬øĆĀ±“śĢžÕōĘų¶Ō¼×ĶéµÄĻą¶ŌĆܶȏĒ11.75£¬ŌņĘäĻą¶Ō·Ö×ÓÖŹĮæĪŖ11.75”Į16=188£¬m=¦ŃV=1.65g•mL-1”Į11.4mL=18.8g£¬øĆÓŠ»śĪļµÄĪļÖŹµÄĮæn=$\frac{m}{M}$=$\frac{18.8g}{188g/mol}$0.1mol£¬BrµÄĪļÖŹµÄĮæÓėĀ±“śĢžµÄĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ1£¬ĖłŅŌĀ±“śĢžÖŠµÄBrŌ×ÓŹżÄæĪŖ2£»
Ā±“śĢžÖŠµÄBrŌ×ÓŹżÄæĪŖ2£¬ĘäĻą¶Ō·Ö×ÓÖŹĮæĪŖ188£¬ĖłŅŌ·Ö×ÓÖŠĢž»łµÄŹ½ĮæĪŖ188-80”Į2=28£¬Ģž»łµÄŹ½Įæ³żŅŌ12£¬ÉĢĪŖĢ¼Ō×ÓŹż£¬ÓąŹżĪŖĒāŌ×ÓŹż£¬ĖłŅŌøĆĢž»łĪŖ-C2H4£¬ĖłŅŌĀ±“śĢžµÄ·Ö×ÓŹ½ĪŖC2H4Br2£¬ĖłŅŌĘä½į¹¹¼ņŹ½ĪŖ£ŗCH2BrCH2Br”¢CH3CHBr2£®
¹Ź“š°øĪŖ£ŗ2£»CH2BrCH2Br”¢CH3CHBr2£®
µćĘĄ ±¾Ģāæ¼²éĮĖĢ½¾æĪļÖŹ×é³ÉµÄ·½·Ø£¬Éę¼°ĮĖĀ±“śĢžµÄĖ®½āŌĄķ”¢Ā±“śĢž·Ö×ÓŹ½”¢½į¹¹¼ņŹ½µÄČ·¶ØµČÖŖŹ¶£¬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāÕĘĪÕĀ±“śĢžµÄĖ®½āŌĄķ¼°¼ģŃé·½·Ø£¬£Ø4£©ĪŖÄŃµć”¢Ņדķµć£¬×¢ŅāĆ÷Č·Č·¶ØĶ黳µÄ·½·Ø£ŗĢž»łµÄŹ½Įæ³żŅŌ12£¬ÉĢĪŖĢ¼Ō×ÓŹż£¬ÓąŹżĪŖĒāŌ×ÓŹż£®


 Š”ѧʌĩ±ź×¼ŹŌ¾ķĻµĮŠ“š°ø
Š”ѧʌĩ±ź×¼ŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼ÓČėµÄ¼īČÜŅŗĢå»ż“ó | B£® | ĖįŗĶ¼īČÜŅŗĢå»żĻąµČ | ||
| C£® | ¼ÓČėµÄ¼īČÜŅŗĢå»żŠ” | D£® | ŅŌÉĻĒéæö¶¼ÓŠæÉÄÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
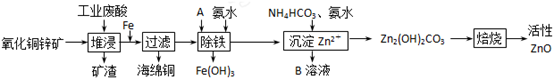
| Ąė×Ó | æŖŹ¼³ĮµķŹ±µÄpH | ĶźČ«³ĮµķŹ±µÄpH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3.36 L | B£® | 4.48 L | C£® | 5.6 L | D£® | 6.72 L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
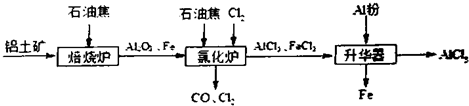
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
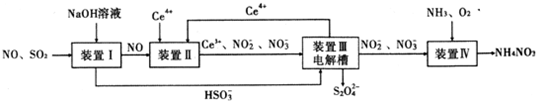
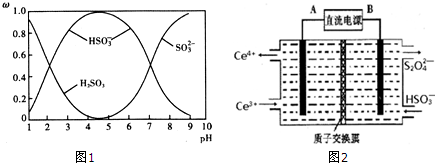
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
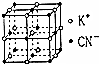 ĮłĒčŗĻĢś£Ø¢ó£©Ėį¼ŲK3[Fe£ØCN£©6]Ė×³Ę³ąŃŖŃĪ£¬ŌŚŅ½Ņ©¹¤Ņµ”¢Ó”Č¾¹¤Ņµ¼°øÖĢś¹¤Ņµ¾łÓŠÖŲŅŖ×÷ÓĆ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ĮłĒčŗĻĢś£Ø¢ó£©Ėį¼ŲK3[Fe£ØCN£©6]Ė×³Ę³ąŃŖŃĪ£¬ŌŚŅ½Ņ©¹¤Ņµ”¢Ó”Č¾¹¤Ņµ¼°øÖĢś¹¤Ņµ¾łÓŠÖŲŅŖ×÷ÓĆ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4ŗĶC3H6 | B£® | C2H4ŗĶC2H6 | C£® | CH4ŗĶC3H4 | D£® | CH4ŗĶC2H4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com