
【题目】一定温度下在甲、乙、丙三个体积相等且恒容的密闭容器中发生反应:NO2(g)+SO2(g) ![]() SO3(g)+NO(g)。投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列说法正确的是
SO3(g)+NO(g)。投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列说法正确的是
起始浓度 | 甲 | 乙 | 丙 |
c(NO2)/(mol·L-1) | 0.10 | 0.20 | 0.20 |
c(SO2)/(mol·L-1) | 0.10 | 0.10 | 0.20 |
A. 容器甲中的反应在前2min的平均速率v(NO)=0.05mol·L-1·min-1
B. 容器乙中若起始时改充0.10mol·L-1NO2和0.20mol·L-1SO2,达到平时c(NO)与原平衡相同
C. 达到平衡时,容器丙中SO3的体积分数是容器甲中SO3的体积分数的2倍
D. 达到平衡时,容器乙中NO2的转化率和容器丙中NO2的转化率相同
【答案】B
【解析】甲经2min达平衡时,NO2的转化率为50%,其平衡浓度为0.05mol/L,
NO2(g)+SO2(g)SO3(g)+NO(g)
开始(mol/L):0.1 0.1 0 0
转化(mol/L):0.05 0.05 0.05 0.05
平衡(mol/L):0.05 0.05 0.05 0.05
故该温度下平衡常数K=![]() ,各容器内温度相同,平衡常数均相同。
,各容器内温度相同,平衡常数均相同。
A.根据v=![]() 计算; B. 据平衡常数的计算式推断;C.该反应为反应前后气体的物质的量不变的反应,容器丙中SO3的体积分数和容器甲中SO3的体积分数相等;D. 单纯的增大某一种物质的浓度,这种物质的转化率一定降低,因此达到平衡时,容器乙中NO2的转化率小于容器丙中NO2的转化率.
计算; B. 据平衡常数的计算式推断;C.该反应为反应前后气体的物质的量不变的反应,容器丙中SO3的体积分数和容器甲中SO3的体积分数相等;D. 单纯的增大某一种物质的浓度,这种物质的转化率一定降低,因此达到平衡时,容器乙中NO2的转化率小于容器丙中NO2的转化率.
A.容器甲中的反应在前2min ,NO的平均速率v(NO)=![]() =0.025mol·L-1·min-1,故A错误;B. 令平衡时NO的浓度为ymol/L,
=0.025mol·L-1·min-1,故A错误;B. 令平衡时NO的浓度为ymol/L,
NO2(g)+SO2(g)SO3(g)+NO(g).
开始(mol/L): 0.1 0.2 0 0
转化(mol/L): y y y y
平衡(mol/L): 0.1-y 0.2-y y y
则![]() ,只要二氧化氮和二氧化硫的浓度分别是0.1mol/L和0.2mol/L,平衡时NO的浓度就相同,故B正确;C.该反应为反应前后气体压强不变的反应,容器丙的反应物的起始浓度是容器甲的2倍,平衡不移动,因此容器丙中SO3的体积分数和容器甲中SO3的体积分数相等,故C错误;D.起始浓度容器乙中的NO2是器甲的2倍,而SO2的起始浓度一样,单纯的增大某一种物质的浓度,这种物质的转化率一定降低,因此达到平衡时,容器乙中NO2的转化率小于容器丙中NO2的转化率,故D错误;答案选B.
,只要二氧化氮和二氧化硫的浓度分别是0.1mol/L和0.2mol/L,平衡时NO的浓度就相同,故B正确;C.该反应为反应前后气体压强不变的反应,容器丙的反应物的起始浓度是容器甲的2倍,平衡不移动,因此容器丙中SO3的体积分数和容器甲中SO3的体积分数相等,故C错误;D.起始浓度容器乙中的NO2是器甲的2倍,而SO2的起始浓度一样,单纯的增大某一种物质的浓度,这种物质的转化率一定降低,因此达到平衡时,容器乙中NO2的转化率小于容器丙中NO2的转化率,故D错误;答案选B.


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
【题目】辉铜矿(主要成分为Cu2S)经火法冶炼,可制得Cu和H2SO4,流程如下图所示:
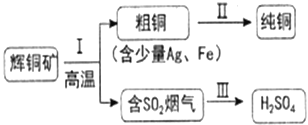
(1)Cu2S中Cu元素的化合价是__________价。
(2)Ⅱ中,电解法精炼粗铜(含少量Ag、Fe),CuSO4溶液做电解质溶液:
①粗铜应与直流电源的_________极(填“正”或“负”)相连。
②铜在阴极析出,而铁以离子形式留在电解质溶液里的原因是__________________________。
(3)Ⅲ中,烟气(主要含SO2、CO2)在较高温度经下图所示方法脱除SO2,并制得H2SO4。
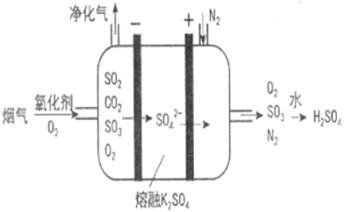
①在阴极放电的物质________________。
②在阳极生成SO3的电极反应式是_______________________________。
(4)检测烟气中SO2脱除率的步骤如下:
(i).将一定量的净化气(不含SO3)通入足量NaOH溶液后,再加入足量溴水。
(ii)加入浓盐酸,加热溶液至无色无气泡,再加入足量BaCl2溶液。
(iii)过滤、洗涤、干燥,称量沉淀质量。
①用离子方程式表示(i)中溴水的主要作用________________________________。
②若沉淀的质量越大,说明SO2的脱除率越________(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯吡格雷是一种用于预防和治疗因血小板高聚集引起的心、脑及其他动脉循环障碍疾 病的药物。以2氯苯甲醛为原料合成该药物的路线如下:

(1)A中官能团名称为_____,A发生银镜反应的化学方程式为_____。
(2)C生成D的反应类型为_____。
(3)X(C6H7BrS)的结构简式为_____。
(4)写出C聚合成高分子化合物的化学反应方程式:_____。
(5)物质G是物质A的同系物,比A多一个碳原子,符合以下条件的G的同分异构体共有______种。
①除苯环之外无其他环状结构;②能发生银镜反应。 其中核磁共振氢谱中有5个吸收峰,且峰值比为2∶2∶1∶1∶1的结构简式为_____。
(6)已知: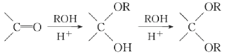 ,写出以乙烯、甲醇为有机原料制备化 合物
,写出以乙烯、甲醇为有机原料制备化 合物![]() 的合成路线(无机试剂任选)__________
的合成路线(无机试剂任选)__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝热反应可用于焊接钢轨,反应为:2Al + Fe2O3 ![]() 2Fe + Al2O3,下列关于该反应说法正确的是
2Fe + Al2O3,下列关于该反应说法正确的是
A. Al 是还原剂 B. Fe2O3 发生氧化反应
C. Fe 是氧化产物 D. 当生成 1 mol Fe 时,转移 6 mol 电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G七种短周期主族元素,它们的原子序数依次增大。B原子的最外层电子数是其次外层电子数的2倍。A的一种原子中,中子数为零。D元素原子的最外层电子数为m=6,次外层电子数为n。E元素原子的L层上电子数为(m+n),M层上电子数为(m/2-n)。F与D同主族。请回答下列问题:
(1)B元素在周期表中的位置是_____,G的离子结构示意图为______
(2)F与G最高价氧化物的水化物的酸性强弱为______>_____(填化学式)
(3)简单D离子和E离子的半径由大到小______>______(填离子符号)
(4)B和D简单气态氢化物的稳定性强弱为_____<_______(填化学式)
(5)F的一种氧化物中氧的质量分数为50%,写出该氧化物与G单质水溶液反应的化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了防止食品受潮及富脂食品氧化变质,在包装袋中应放入的独立包装的物质是
A. 无水硫酸铜、蔗糖 B. 食盐、硫酸亚铁
C. 生石灰、还原铁粉 D. 生石灰、食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上运用电化学方法降解含NO3-废水的原理如图所示,下列有关说法不正确的是

A. 相同条件下,Pt电极上产生O2和Pt-A电极上产生N2的体积比为5:2
B. 通电时电子的流向:b电极→导线→Pt-Ag电极→溶液→Pt电极→导线→a极
C. Pt-Ag电极上的电极反应式:2NO3-+12H++10e-=N2+6H2O
D. 通电时,Pt电极附近溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在溶液中能大量共存的是
A.Na+、OH-、SiO32-、Cl-B.Fe3+、 NH4+、SCN-、Cl-
C.Fe2+ 、H+、Na+ 、MnO4-D.Na+、AlO2-、SO42-、H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com