
| A.氢气和氯气点燃生成氯化氢,氯化氢受热分解为氢气和氯气 |
| B.氮气和氢气在高温、高压、催化剂作用下可以生成氨气,同时氨气又分解为氮气和氢气 |
| C.单质溴可以置换出碘,氯气又可以置换出溴 |
| D.氯气和水反应生成盐酸和次氯酸,次氯酸光照条件下可分解为盐酸和氧气 |
科目:高中化学 来源:不详 题型:单选题
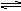 2Z(g) △H<0 ,为了使平衡向生成Z的方向移动,应选择下列的适宜条件是( )
2Z(g) △H<0 ,为了使平衡向生成Z的方向移动,应选择下列的适宜条件是( )| A.①③⑤ | B.②③⑤ | C.②③⑤⑥ | D.②③⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
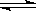 N2O4(g)△H<0。
N2O4(g)△H<0。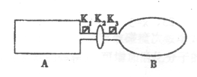
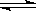 P(g)+Q(g);△H>0,请回答下列问题:①若要增大M的转化率,在其它条件不变的情况下可以采取的措施为
P(g)+Q(g);△H>0,请回答下列问题:①若要增大M的转化率,在其它条件不变的情况下可以采取的措施为 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C+D,在t1时增大压强,则正、逆反应速率变化如图所示(v表示反应速率,t代表时间),下列有关A、B、C、D的状态叙述正确的是
C+D,在t1时增大压强,则正、逆反应速率变化如图所示(v表示反应速率,t代表时间),下列有关A、B、C、D的状态叙述正确的是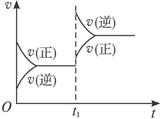
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
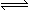 2SO3,2 min时,测得O2的物质的量为1.6 mol,则:
2SO3,2 min时,测得O2的物质的量为1.6 mol,则: (1)2min内,平均反应速率v(O2)= ; v(SO3)= 。
(1)2min内,平均反应速率v(O2)= ; v(SO3)= 。 (2)2min时,SO2的浓度为
(2)2min时,SO2的浓度为  (3)若2min时测得上述反应放出Q kJ的热量,试写出该反应的热化学方程式
(3)若2min时测得上述反应放出Q kJ的热量,试写出该反应的热化学方程式查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
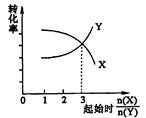
 3Z B 3X+2Y
3Z B 3X+2Y 2Z
2Z Z D 3X+Y
Z D 3X+Y Z
Z查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O Cr3+(aq)+3OH—(aq)。
Cr3+(aq)+3OH—(aq)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
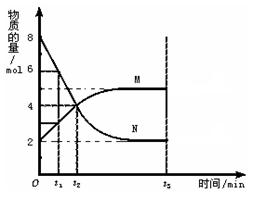
| A.t2时刻该反应达到平衡 |
| B.t3时刻该反应达到平衡 |
| C.反应开始时,生成物的浓度为0 |
| D.该反应的限度是可以改变的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com