
【题目】G是一种常见的氨基酸,其合成路线如下
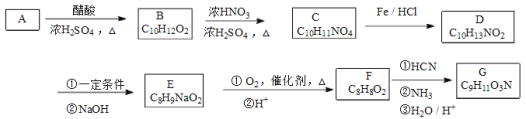
已知以下信息:
①A苯环上只有1个取代基且核磁共振氢谱有6组峰,其面积比为1∶2∶2∶2∶2∶1;D和F的苯环上的一氯代物都只有2种;
②F、G能与FeCl3溶液发生显色反应,F能发生银镜反应;
③![]()
④
回答下列问题
(1)A的分子式为__________,其名称为__________。
(2)A→B的反应类型是__________;鉴别A和B可用的试剂是__________。
(3)B→C的化学方程式为________________________。
(4)G的结构简式为__________。
(5)F的同分异构构体,含有苯环且能发生水解反应的异构体有__________种,其中核磁共振氢谱有4组峰,且面积比为3:2:2:1的是__________。
【答案】C8H10O 苯乙醇 取代反应(酯化反应) 金属钠 ![]() +HNO3
+HNO3![]()
![]() +H2O
+H2O  6
6 ![]() 或
或![]() 或
或![]()
【解析】
据A与乙酸发生酯化反应,生成B的分子式结合信息①可知A为苯乙醇,分子式为C8H10O,据反应条件可知A与乙酸发生酯化反应,生成的B为 ,B→C为硝化反应,D和F的苯环上的一氯代物都只有2种,说明在对位取代,C为
,B→C为硝化反应,D和F的苯环上的一氯代物都只有2种,说明在对位取代,C为 ,C→D的反应是硝基还原为氨基的反应,F、G能与FeCl3溶液发生显色反应,F能发生银镜反应,可知D→E是酯的水解反应和氨基生成羟基的反应,E为
,C→D的反应是硝基还原为氨基的反应,F、G能与FeCl3溶液发生显色反应,F能发生银镜反应,可知D→E是酯的水解反应和氨基生成羟基的反应,E为 ,E氧化后酸化生成F,F能发生银镜反应,F为
,E氧化后酸化生成F,F能发生银镜反应,F为 ,据信息③可知,G为
,据信息③可知,G为 ,据此分析。
,据此分析。
(1)据解析可知,A的分子式为C8H10O,名称是苯乙醇;
(2)据反应条件可知A与乙酸发生酯化反应,生成的B为乙酸苯乙酯,用金属Na可以鉴别A与B,A与Na反应生成气体,B不能;
(3)B→C为硝化反应,D和F的苯环上的一氯代物都只有2种,说明在对位取代,C为 ,反应方程式为:
,反应方程式为:  +HNO3
+HNO3![]()
 +H2O;
+H2O;
(4)F为 ,据信息③可知,G为
,据信息③可知,G为 ;(5)F为
;(5)F为 ,其含有苯环且能发生水解反应的异构体中需有酯基,可以是酚羟基与甲酸形成的酯,另有一个甲基,这样的酯有邻、间、对3种,可以是酚羟基与乙酸形成的酯,有1种,苯甲酸与甲醇形成的酯,有1种,苯甲醇与甲酸形成的酯,有1种,共6种,其中核磁共振氢谱有4组峰,且面积比为3:2:2:1的是
,其含有苯环且能发生水解反应的异构体中需有酯基,可以是酚羟基与甲酸形成的酯,另有一个甲基,这样的酯有邻、间、对3种,可以是酚羟基与乙酸形成的酯,有1种,苯甲酸与甲醇形成的酯,有1种,苯甲醇与甲酸形成的酯,有1种,共6种,其中核磁共振氢谱有4组峰,且面积比为3:2:2:1的是![]() 或
或![]() 或
或![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】有机物J是合成药物格列卫的一种重要中间体,J的一种合成路线如下:

已知:①
②R-NH2 R-NH2
R-NH2
回答下列问题:
(1)B的名称为________。
(2)H→I和I→J的反应类型分别为________、________。
(3)G的结构简式为________。
(4)由E生成F的化学方程式为_______________________________________________。
(5)芳香化合物X是E的同分异构体,X能发生银镜反应,并能发生水解反应,其核磁共振氢谱有4组峰,峰面积之比为1∶4∶2∶1,写出符合条件的X的结构简式________________
(6)写出用甲苯为原料制备聚合物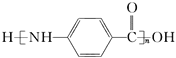 的合成路线:_______________
的合成路线:_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,满足表中图示物质在一定条件下能一步转化的组合有
序号 | X | Y | Z | W |
|
① | Cu | CuSO4 | Cu(OH)2 | CuO | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Al | AlCl3 | Al(OH)3 | Al2O3 | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A.①②③B.①③④C.①②④D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀。
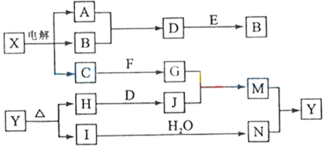
请回答下列问题:
(1)A在B中燃烧的现象是__________________________________________。
(2)D+E→B的反应中,被氧化与被还原的物质的物质的量比是_________________________。
(3)G+J→M的离子方程式是____________________________________。
(4)Y受热分解的化学方程式是______________________________________。
(5)检验硫酸铁溶液中是否存在Fe2+的试剂是 ____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等杂质)制取金属锌的工艺流程如下。回答下列问题:
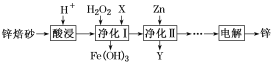
(1)ZnFe2O4是一种性能优良的软磁材料,也是一种催化剂,能催化烯类有机物氧化脱氢等反应。
①ZnFe2O4中Fe的化合价是________。
②工业上利用反应ZnFe2(C2O4)3·6H2O![]() ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中每生成1 mol ZnFe2O4转移电子的物质的量是________。
ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中每生成1 mol ZnFe2O4转移电子的物质的量是________。
(2)酸浸时要将锌焙砂粉碎,其目的是提高酸浸效率。为达到这一目的,还可采用的措施是________________________(任答一条);已知ZnFe2O4能溶于酸,则酸浸后溶液中存在的金属离子有____________________________________________。
(3)净化Ⅰ中H2O2参与反应的离子方程式为_________;试剂X的作用是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是一种金属,B溶液能使酚酞试液变红,且焰色反应呈黄色;D、F相遇会产生白烟。A、B、C、D、E、F间有如图变化关系:

(1)A的名称是______________;F的化学式是______________。
(2)B→D反应的化学方程式为________________________。
(3)F+D→C反应的化学方程式为__________________________。
(4)F在空气中遇水蒸气产生白雾现象,这白雾实际上是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 甲苯可以与液溴混合后加入铁粉生成![]()
B. 实验室制备乙烯时,温度计水银球应该插入浓硫酸和无水乙醇的混合液液面以下
C. 向溴乙烷中加入NaOH溶液加热,充分反应,再加入AgNO3溶液,产生淡黄色沉淀,证明溴乙烷中含有溴元素
D. 制备新制Cu(OH)2悬浊液时,将4~6滴2%的NaOH溶液滴入2mL2%的CuSO4溶液中,边滴边振荡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组同学对乙醛与新制的Cu(OH)2反应的实验进行探究。
实验Ⅰ:取2mL 10%的氢氧化钠溶液于试管中,加入5滴2%的CuSO4溶液和5滴5%的乙醛溶液,加热时蓝色悬浊液变黑,静置后未发现红色沉淀。
实验小组对影响实验Ⅰ成败的因素进行探究:
(1)探究乙醛溶液浓度对该反应的影响。
编号 | 实验Ⅱ | 实验Ⅲ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变红棕色,静置后底部有大量红色沉淀 | 加热,蓝色悬浊液变红棕色,静置后上层为棕黄色油状液体,底部有少量红色沉淀 |
已知:乙醛在碱性条件下发生缩合反应:CH3CHO+CH3CHO![]() CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
① 能证明乙醛被新制的Cu(OH)2 氧化的实验现象是______。
② 乙醛与新制的Cu(OH)2 发生反应的化学方程式是______。
③ 分析实验Ⅲ产生的红色沉淀少于实验Ⅱ的可能原因:______。
(2)探究NaOH溶液浓度对该反应的影响。
编号 | 实验Ⅳ | 实验Ⅴ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变黑 | 加热,蓝色悬浊液变红棕色, 静置后底部有红色沉淀 |
依据实验Ⅰ→Ⅴ,得出如下结论:
ⅰ. NaOH溶液浓度一定时,适当增大乙醛溶液浓度有利于生成Cu2O。
ⅱ. 乙醛溶液浓度一定时,______。
(3)探究NaOH溶液浓度与乙醛溶液浓度对该反应影响程度的差异。
编号 | 实验Ⅵ | 实验Ⅶ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变黑 | 加热,静置后底部有红色沉淀 |
由以上实验得出推论: ______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com