
| A. | 100 mL 1 mol/L的FeCl3溶液完全生成Fe(OH)3胶体,其胶粒数目为0.1 NA | |
| B. | 7.8 gNa2O2中含有的离子总数目为0.4 NA | |
| C. | 标准状况下,44.8 L HF所含分子数为2 NA | |
| D. | 标准状况下,80 gSO3中所含的原子数为4 NA |
分析 A、一个胶粒是多个氢氧化铁的聚集体;
B、求出过氧化钠的物质的量,然后根据1mol过氧化钠中含2mol钠离子和1mol过氧根来分析;
C、标况下HF为液态;
D、求出三氧化硫的物质的量,然后根据1mol三氧化硫中含4mol原子来分析.
解答 解:A、一个胶粒是多个氢氧化铁的聚集体,故得到的氢氧化铁胶粒的个数小于0.1NA个,故A错误;
B、7.8g过氧化钠的物质的量为0.1mol,而1mol过氧化钠中含2mol钠离子和1mol过氧根,故0.1mol过氧化钠中含0.3NA个离子,故B错误;
C、标况下HF为液态,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D、80g三氧化硫的物质的量为1mol,而1mol三氧化硫中含4mol原子,即4NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
 “天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将太阳能电池电解水技术与氢氧燃料电池技术相结合的可充电电池.下图为RFC工作原理示意图(隔膜为质子选择性透过膜),下列说法中正确的是( )
“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将太阳能电池电解水技术与氢氧燃料电池技术相结合的可充电电池.下图为RFC工作原理示意图(隔膜为质子选择性透过膜),下列说法中正确的是( )| A. | c极上发生的电极反应是:O2+4H++4e-═2H2O | |
| B. | 当有0.1mol电子转移时,b极产生1.12L 气体Y(标准状况下) | |
| C. | 装置I与装置II的电解质溶液中,氢离子运动方向相反 | |
| D. | RFC系统工作过程中只存在3种形式的能量转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
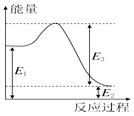 甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.已知:
甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.已知:| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能 (kJ•mol-1) | 348 | 413 | 436 | 358 | 1072 | 463 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | |
| Y | Z |
| A. | 若 X 通过共用三对电子可形成 X2 分子,Z 在周期表中的位置是第三周期Ⅵ族 | |
| B. | 若 X、Y、Z 都是金属,则它们的最高价氧化物的水化物都是强碱 | |
| C. | 若它们原子最外层电子数之和为 13,则它们均为非金属元素 | |
| D. | 若 X、Y、Z 都是非金属,则三者形成的简单氢化物中,Z 的氢化物沸点最高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
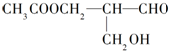 在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性,下面的物质有光学活性:发生下列反应后生成的有机物无光学活性的是( )
在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性,下面的物质有光学活性:发生下列反应后生成的有机物无光学活性的是( )| A. | 与甲酸发生酯化反应 | B. | 与新制的氢氧化铜作用 | ||
| C. | 与银氨溶液作用 | D. | 在催化剂存在下与H2作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 天平所配的砖码有脏污 | |
| B. | 药品保存不善,露置时间过长 | |
| C. | 定容时液面与容量瓶壁交界处到达刻度就定容完毕 | |
| D. | 溶解步骤完成后,洗涤次数过多 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Ksp(AB2)<Ksp(CD),说明AB2的溶解度小于CD的溶解度 | |
| B. | 在ZnS的沉淀溶解平衡体系中加入蒸馏水,ZnS的Ksp不变 | |
| C. | 已知Ksp(AgCl)>Ksp(AgI),则反应AgCl(s)+I-(aq)=AgI(s)+Cl-(aq)能够发生 | |
| D. | 在CaCO3的沉淀溶解平衡体系中加入稀盐酸,沉淀溶解平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
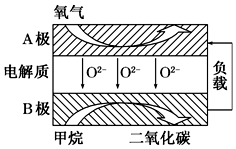 以甲烷为燃料的新型电池得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池的工作原理示意图.下列说法错误的是( )
以甲烷为燃料的新型电池得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池的工作原理示意图.下列说法错误的是( )| A. | 以甲烷为燃料,其成本大大低于以氢气为燃料的传统燃料电池 | |
| B. | A电极为电池正极,发生还原反应 | |
| C. | B电极反应式为CH4+4O2--8e-═CO2+2H2O | |
| D. | 若用该燃料电池作电源,用石墨作电极电解100 mL 1 mol•L-1的硫酸铜溶液,当两极收集到的气体体积相等时,理论上消耗的甲烷的体积为22.4L(标准状况下) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com