
(16分)某小组进行铝热反应实验,装置如图所示。
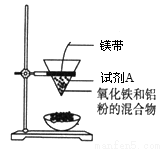
(1)铝热反应原理 (写化学方程式),试剂A为 (写化学式)。
(2)对坩埚内的黑色固体物质的组成,小组进行了如下探究
假设I:该黑色物质为铁
假设Ⅱ:该黑色物质为铁与氧化铁的混合物
【设计方案并实验】
实 验 步 骤 | 现 象 | 结 论 |
①取少量黑色固体于试管中加稀盐酸 | 固体全部溶解,有气泡产生 | 假设I成立,假设Ⅱ不成立 |
②滴入几滴0.01mol/LKSCN溶液 | 溶液不变色 |
【交流评价】
你认为上述结论是否合理? ,理由是 。
(3)取上述实验所得溶液,滴入适量氯水溶液变红色。
①此时涉及的氧化还原反应的离子反应方程式为 。
②利用反应体系中存在的平衡:Fe3++3SCN— Fe(SCN)3,小组再将滴入适量氯水的溶液平均分成两份,分别置于两支试管中并编号l、2,进行如下表所示的探究。该实验中,小组主要探究的问题是 ;应重点观察的现象是 ;预计得出的结论是 。
Fe(SCN)3,小组再将滴入适量氯水的溶液平均分成两份,分别置于两支试管中并编号l、2,进行如下表所示的探究。该实验中,小组主要探究的问题是 ;应重点观察的现象是 ;预计得出的结论是 。
实验编号 | 实验步骤 |
1 | ①滴加饱和FeCl3溶液4滴,充分振荡 |
②滴加几滴NaOH溶液 | |
2 | ①滴加4滴1mol/LKSCN溶液 |
②滴加几滴NaOH溶液 |
(16分)(1)Fe2O3+2Al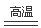 2Fe+Al2O3(3)KClO3(2分)
2Fe+Al2O3(3)KClO3(2分)
(2)不合理(1分)Fe2O3与酸反应生成的Fe3+与Fe反应生成Fe2+,滴入KSCN溶液后也不变色(2分)
(3)①2Fe2++Cl2=2Fe3++2Cl-(2分)②反应物浓度(或浓度)对化学平衡移动的影响(2分)溶液颜色的变化(2分)增大(或减小)反应物的浓度,平衡向正(或逆)反应方向移动(2分)
【解析】
试题分析:(1)铝热反应原理是在加热条件下Al与金属氧化物发生置换反应,把金属从化合物中置换出来,对于该反应来说,铝热反应的方程式为:Fe2O3+2Al 2Fe+Al2O3;为了防止插入固体混合物中的镁带不能引燃该反应,在铝热剂上边铺了一层强氧化剂KClO3,所以试剂A是KClO3;(2)只要发生反应,就会产生金属铁,若反应不完全,当把反应后的固体加入盐酸时,会发生反应:Fe+2HCl=FeCl2+H2↑;Fe2O3+6HCl=2FeCl3+3H2O;2FeCl3+Fe=3 FeCl2;当加入KSCN溶液时,溶液也不会为红色,因此该说法是错误的;(3)取上述实验所得溶液,滴入适量氯水溶液变红色。①此时涉及的氧化还原反应的离子反应方程式为2Fe2++Cl2=2Fe3++2Cl-;②该实验就是通过增大反应物浓度或减小生成物的浓度,共存溶液的颜色变化来探究反应物浓度(或浓度)对化学平衡移动的影响;在其它条件不变时,增大反应物的浓度或减小生成物的浓度,平衡正向移动;减小反应物的浓度或增大生成物的浓度,平衡向逆反应方向移动。
2Fe+Al2O3;为了防止插入固体混合物中的镁带不能引燃该反应,在铝热剂上边铺了一层强氧化剂KClO3,所以试剂A是KClO3;(2)只要发生反应,就会产生金属铁,若反应不完全,当把反应后的固体加入盐酸时,会发生反应:Fe+2HCl=FeCl2+H2↑;Fe2O3+6HCl=2FeCl3+3H2O;2FeCl3+Fe=3 FeCl2;当加入KSCN溶液时,溶液也不会为红色,因此该说法是错误的;(3)取上述实验所得溶液,滴入适量氯水溶液变红色。①此时涉及的氧化还原反应的离子反应方程式为2Fe2++Cl2=2Fe3++2Cl-;②该实验就是通过增大反应物浓度或减小生成物的浓度,共存溶液的颜色变化来探究反应物浓度(或浓度)对化学平衡移动的影响;在其它条件不变时,增大反应物的浓度或减小生成物的浓度,平衡正向移动;减小反应物的浓度或增大生成物的浓度,平衡向逆反应方向移动。
考点:考查铝热反应原理及应用、物质的确定及作用、实验方案的设计与评价、反应条件的分析及影响、离子方程式的书写的知识。


科目:高中化学 来源:2014-2015湖南省娄底市高二上学期期末考试化学(文)试卷(解析版) 题型:选择题
“每天一个苹果,医生远离我”,说明苹果对人体健康非常有益,苹果为人体提供的主要营养素是
A.油脂 B.无机盐 C.蛋白质 D.维生素
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省娄底市高一上学期期末考试化学试卷(解析版) 题型:选择题
对I~IV的实验操作现象判断正确的是

A.实验I:产生红褐色沉淀
B.实验II:溶液颜色变红
C.实验III:放出大量气体
D.实验IV:先出现白色沉淀,后沉淀又溶解
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省娄底市高二上学期期末考试化学(理)试卷(解析版) 题型:选择题
以下现象与电化学腐蚀无关的是:
A.黄铜(铜锌合金)制作的铜锣不易产生铜绿
B.生铁比纯铁更易生锈
C.铁质配件附有铜质配件,在接触处易生铁锈
D.银质物品久置表面变暗
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省娄底市高二上学期期末考试化学(理)试卷(解析版) 题型:选择题
2A(g)+B(g) 3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是
3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是
A.V(A) = 0.7mol·L-1·min-1
B.V(B) = 0.3mol·L-1·min-1
C.V(C) = 0.9mol·L-1·min-1
D.V(D) = 1.1mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省清远市高三上学期期末理综化学试卷(解析版) 题型:选择题
下图所示的五种元素中,W、X、Y、Z为短周期元素,X元素的单质是空气中含量最多的成分。下列说法正确的是
X | Z[ | ||
T |
A.X位于元素周期表中第二周期ⅤA族
B.X、Y、Z三种元素的气态氢化物的稳定性依次减弱
C.由X、Y和氢三种元素形成的化合物中只有共价键
D.元素T与X的原子序数相差25
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省茂名市高三一模考试理综化学试卷(解析版) 题型:实验题
研究性学习小组利用下列有关装置进行探究实验,回答相关问题。

(1)写出A中的反应化学方程式
(2)实验时,旋开装置A中分液漏斗的旋塞,发现液体流出缓慢,最终停止,其可能的原因是 。
(3)装置B中的溶液出现浑浊,该实验证明SO2具有 性 。
(4)实验后,测定装置C中溶液呈碱性。溶液为什么呈碱性呢?大家有不同意见:①是生成的Na2SO3水解;②是氢氧化钠剩余。请设计实验方案证明哪种意见成立。选用下列试剂进行实验:Na2SO3溶液、酚酞溶液、氯水、BaCl2溶液、稀硫酸
实验步骤 | 实验操作 | 预期现象与结论 |
(5)另一小组利用装置D进行实验:用注射器向装置D共注入v mL实验室制备SO2的空气,当溶液刚好褪色,停止实验。

该小组的实验目的是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省部分普高高三2月联考化学试卷(解析版) 题型:填空题
(12分)某强酸性溶液X中仅含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下:

根据以上信息,回答下列问题:
(1)仅根据上述连续实验不能确定溶液X中是否含有的阳、阴离子分别是_____________。
(2)用离子方程表达下列反应:
①中生成气体A:___________ __。
②中生成溶液H:____________ _。
(3)若②中所用氢氧化钠浓度为2mol/L,当加入l0 ml时开始产生沉淀,55 ml时沉淀的量达到最大值0.03 mol,继续滴加沉淀的量保持不变,随后再滴加沉淀部分溶解,到60ml时沉淀的量降为0.025 mol且保持不变,则原溶液中c(Fe2+)为___________mol/L、c(Fe3+)为___________mol/L、c(Cl-)为___________mol/L。(若有些离子不存在,请填0 mol/L)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期期末考试化学试卷(解析版) 题型:选择题
TESLA电动汽车的电池采用了松下提供的NCA系列(镍钴铝体系)的18650A型钴酸锂(LiCoO2)锂离子电池。电池正极材料为钴酸锂(LiCoO2),负极材料是石墨(C6)。电池反应为: LiCoO2+C6 C6Lix+Li1-xCoO2。下列有关说法不正确的是
C6Lix+Li1-xCoO2。下列有关说法不正确的是
A.锂离子电池与传统铅蓄电池相比,具有高比能量(比能量指的是单位重量或单位体积的能量)的特点
B.废旧锂离子电池先进行“放电处理”让Li+进入石墨(C6)中而利于回收
C.放电时,正极锂的化合价未发生改变
D.充电时电池正极上发生的反应为:LiCoO2—x e-=== Li1-x CoO2+xLi+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com