
分析 (1)根据n=$\frac{V}{{V}_{m}}$计算HCl物质的量,再根据c=$\frac{n}{V}$计算盐酸的物质的量浓度;
(2)根据n=$\frac{m}{M}$计算Zn的物质的量,根据方程式计算需要HCl的物质的量,再根据V=$\frac{n}{c}$计算需要盐酸的体积.
解答 解:(1)标况下3.36L HCl的物质的量为$\frac{33.6L}{22.4L/mol}$=1.5mol,盐酸的物质的量浓度为$\frac{1.5mol}{0.25L}$=6mol/L,
答:该盐酸的物质的量浓度为6mol/L;
(2)19.5g Zn的物质的量为$\frac{19.5g}{65g/mol}$=0.3mol,根据方程式:Zn+2HCl=ZnCl2+H2↑,可知需要HCl的物质的量为0.3mol×2=0.6mol,故需要盐酸的最小体积为$\frac{0.6mol}{6mol/L}$=0.1L,
答:需要该盐酸的最小体积为0.1L.
点评 本题考查物质的量有关计算、化学方程式计算,比较基础,有利于基础知识的巩固.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 凉拌青菜、土豆丝、馒头 | |
| B. | 虾仁白菜、红烧带鱼、酸菜炖猪蹄、萝卜汤 | |
| C. | 糖醋排骨、清蒸鲈鱼、米饭 | |
| D. | 酱牛肉、炒油菜、红烧豆腐、西红柿蛋汤、馒头 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
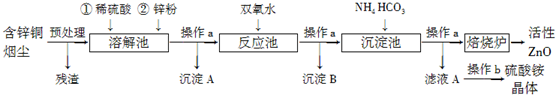
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液+AgNO3溶液→生成白色沉淀,说明原溶液中有Cl- | |
| B. | 某溶液+BaCl2溶液→生成白色沉淀,说明原溶液中有SO42- | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ | |
| D. | 某溶液+稀硫酸→生成无色气体,该气体能使澄清石灰水变浑浊,则原溶液中有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
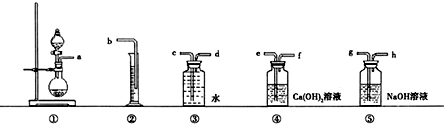
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
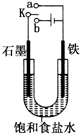 某课外活动小组同学用如图装置进行实验,试回答下列问题:
某课外活动小组同学用如图装置进行实验,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O4的摩尔质量是64 g | |
| B. | O4与O2互为同位素 | |
| C. | O4与O3、O2都是氧元素的同分异构体 | |
| D. | 相同质量的O4与O3所含原子个数之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com