
����Ŀ������ѡ���У��������ʵ�����ģ������������ޣ��ܹ������Ӧʵ�����
ѡ�� | ʵ������ | ��Ӧʵ�� |
A | ̽����ѧ��Ӧ���� | ȡ5mL0��1mol/LKI��Һ���μ�0��1mol/L FeCl3��Һ5~6�Σ��ɸ�����Һ�мȺ�I2�ֺ���I-��ʵ����ʵ�жϸ÷�Ӧ�ǿ��淴Ӧ |
B | ̽�����ԣ�HCO 3 -��Al(OH) 3 | ��NaHCO3��Һ�еμ�NaAlO2��Һ���۲��Ƿ��а�ɫ�������� |
C | ̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�� | ����ֻ�Թܸ�ȡ5mL0��1mol/LKMnO4��Һ���ֱ����2mL0��1mol/L��1mL0��2mol/LH 2C 2O 4��Һ����¼��Һ��ɫ����Ҫ��ʱ�� |
D | ̽�������ԣ�Cl 2��Br 2��I2 | ��NaBr��Һ�еμ���ˮ���ټ������KI��Һ����Һ���� |
A. A B. B C. C D. D
���𰸡�B
��������A��KI��FeCl3����������ԭ��Ӧ�������ӷ�ӦΪ2Fe3����2I��=2Fe2����I2����ΪKI�ǹ����������Һ�д���I����I2������˵����Ӧ�ǿ��淴Ӧ����A����B. ��NaHCO3��Һ�еμ�NaAlO2��Һ��������ӦΪ��NaAlO2+ NaHCO3+H2O= Na2CO3+ Al(OH) 3![]() ������ɫ����,˵�����ԣ�HCO 3 -��Al(OH) 3����B ��ȷ��C�����Ը��������Һ����ᷴӦ�����ӷ���ʽΪ��2MnO4����5H2C2O4��6H��=8H2O��10CO2����2Mn2������Ϊ������ع�����������Һ����ɫ����C����D.��NaBr��Һ�еμ���ˮ��Ӧ����ʽ��2 Br-+Cl2= Br2+2Cl-�ټ������KI��Һ����Ϊ�������嶼���ѵ���������Ϊ�ⵥ�ʣ�ʹ������Һ��������D���𰸣�B��
������ɫ����,˵�����ԣ�HCO 3 -��Al(OH) 3����B ��ȷ��C�����Ը��������Һ����ᷴӦ�����ӷ���ʽΪ��2MnO4����5H2C2O4��6H��=8H2O��10CO2����2Mn2������Ϊ������ع�����������Һ����ɫ����C����D.��NaBr��Һ�еμ���ˮ��Ӧ����ʽ��2 Br-+Cl2= Br2+2Cl-�ټ������KI��Һ����Ϊ�������嶼���ѵ���������Ϊ�ⵥ�ʣ�ʹ������Һ��������D���𰸣�B��


 �ƸԹھ��ο���ϵ�д�
�ƸԹھ��ο���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���� (����)
A. HF��HCl��H2S��PH3���ȶ���������ǿ
B. ��Mg��Si��N��F��˳��ԭ�Ӱ뾶��С���
C. ij����Ԫ�صĵ�����I1��I7�������±���ʾ(��λ��kJ/mol)�����Ʋ��Ԫ��λ��Ԫ�����ڱ��ڢ�A��

D. �ڢ�P��S����Mg��Ca����Al��Si����Ԫ���У�ÿ���е�һ�����ܽϴ��Ԫ�ص�ԭ������֮��Ϊ41
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ϸ�������������ٷֱ���������Ԫ���ǣ� ��
A.C��HB.H��OC.C��OD.C��N
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Դ�����ͬ��ע����Ҫ���⡣ҳ�����Ǵ�ҳ�Ҳ��п��ɳ�����һ�ַdz���Ҫ����Ȼ����Դ��ҳ��������Ҫ�ɷ��Ǽ��飬�ǹ��ϵĽྻ��Դ��
��1��ҳ��������������ȼ�ϣ��������������ϳ���(CO��H2)��CH4��H2O(g)ͨ��۽�̫���ܷ�Ӧ����������Ӧ CH4(g)+H2O(g)=CO(g)+3H2(g)��H1
��֪����CH4��H2��CO ��ȼ���ȣ���H���ֱ�Ϊ-a kJmol-1��-b kJmol-1��-c kJmol-1��
��H2O (l) =H2O(g)�� ��H=+dkJmol-1
����H1= ___________���ú���ĸa��b��c��d�Ĵ���ʽ��ʾ��kJmol-1��
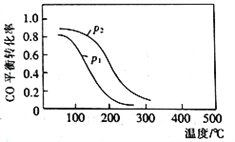
��2���úϳ������ɼ״��ķ�ӦΪ��CO(g)+2H2(g)![]() CH3OH(g) ��H2����10L�����ܱ������а����ʵ���֮��1��2����CO��H2�����CO��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��200��ʱn(H2)��ʱ��ı仯���±���ʾ��
CH3OH(g) ��H2����10L�����ܱ������а����ʵ���֮��1��2����CO��H2�����CO��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��200��ʱn(H2)��ʱ��ı仯���±���ʾ��
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
�١�H2_________ (����>����<������ = ��)0��
������˵����ȷ����____________ (���ţ���
a.�¶�Խ�ߣ��÷�Ӧ��ƽ�ⳣ��Խ��
b.��ƽ����ٳ���ϡ�����壬CO��ת�������
c.����������ѹǿ���ٱ仯ʱ����Ӧ�ﵽ�����
d.ͼ��ѹǿp1<p2
�� 03 min����CH3OH��ʾ�ķ�Ӧ����v(CH3OH)=________mol L-1��min-1��
�� 200��ʱ���÷�Ӧ��ƽ�ⳣ��K =_______��������200���ﵽƽ��ĺ����ܱ��������ټ���2 mol CO��2 mol H2��2 mol CH3OH�������¶Ȳ��䣬��ѧƽ��____________(����������������������������)�ƶ���
��3�����顢������KOH��Һ�����ȼ�ϵ�ء���״����ͨ��5.6 L���飬��õ�·��ת��1.2 mol���ӣ�������������Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Cu��ϡ�����п��Է������·�Ӧ��3Cu+8HNO3��3Cu(NO3)2+2NO��+4H2O ����������ȷ���ǣ���
A. HNO3�ڷ�Ӧ��ʧȥ����
B. ���������뻹ԭ��������ʵ�����Ϊ3:2
C. ����������Ӧ������ռ�μӷ�Ӧ�����1/4
D. ÿ1 mol HNO3�μӷ�Ӧ����3 mol����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±��е��������ƻ�1 mol�����еĻ�ѧ�������ĵ�����(kJ)��
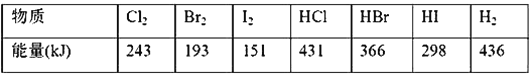
��1���������ʱ������е�������͵�����____��
A��H2 B��Cl2 C��Br2 D��I2
��2�������⻯���У����ȶ�������____��
A��HCl B��HBr C��HI
��3��X2��H2===2HX(X����Cl��Br��I)�ķ�Ӧ�����ȷ�Ӧ���Ƿ��ȷ�Ӧ�� _____________��
��4����ͬ�����£�X2(X����Cl��Br��I)�ֱ���������Ӧ�������ĵ����ʵ���������ʱ���ų������յ�����������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijϩ���������ӳɺ�õ�2��2���������飬���ϩ����������
A. 2��2��������3����ϩ B. 2��2��������2����ϩ
C. 2��2��������1����ϩ D. 3��3��������1����ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ�ڹ�ҵ����Ҫ�������쵼�ߡ�����Ԫ���ȣ�ͭ���γɣ�1�ۺͣ�2�۵Ļ����
(1)д����̬Cu���ĺ�������Ų�ʽ___________________________________��
(2)��ͼ��ͭ��ij��������ľ���ʾ��ͼ����������Ļ�ѧʽΪ________��

(3)������ͭ��Һ�еμӰ�ˮ��������ɫ�������ٵμӰ�ˮ�������պ�ȫ���ܽ�ɵõ�����ɫ��Һ�����������м��뼫�Խ�С���Ҵ�������������ɫ��[Cu(NH3)4]SO4��H2O�������������е�NH3ͨ��________������������Cu2����ϣ�NH3������Nԭ�ӵ��ӻ���ʽ��____����NH3���ӻ�Ϊ�ȵ������һ������________��
(4)CuO���۵��CuCl���۵�____(��ߡ��͡�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaCl��Һ���������ᾧ����ʱ�����в�������ȷ˳���ǣ� ��
�ٷ��þƾ��Ƣڹ̶���Ȧλ�â۷���������ܼ��Ƚ����ֹͣ����,��������
A.�ڢۢܢݢ�
B.�٢ڢۢܢ�
C.�٢ۢڢܢ�
D.�ڢ٢ۢܢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com