
ĻĀĮŠ¹ŲÓŚ·“Ó¦ÄÜĮæµÄĖµ·ØÕżČ·µÄŹĒ£Ø£©
A£® Zn£Øs£©+CuSO4£Øaq£©═ZnSO4£Øaq£©+Cu£Øs£©”÷H=﹣216 kJ/mol£¬Ōņ·“Ó¦Īļ×ÜÄÜĮæ“óÓŚÉś³ÉĪļ×ÜÄÜĮæ
B£® ČōŅ»¶ØĢõ¼žĻĀ£¬A═B”÷H£¼0£¬ĖµĆ÷AĪļÖŹ±ČBĪļÖŹĪȶØ
C£® 101 kPaŹ±£¬2H2£Øg£©+O2£Øg£©═2H2O£Øl£©”÷H=﹣571.6 kJ/mol£¬ŌņH2µÄČ¼ÉÕČČĪŖ571.6 kJ/mol
D£® H+£Øaq£©+OH﹣£Øaq£©═H2O£Øl£©”÷H=﹣57.3 kJ/mol£¬ŗ¬1 molNaOHµÄČÜŅŗÓėŗ¬0.5 mol H2SO4µÄÅØĮņĖį»ģŗĻŗó·Å³ö57.3 kJµÄČČĮæ
æ¼µć£ŗ ·“Ó¦ČČŗĶģŹ±ä£»Č¼ÉÕČČ£»ÖŠŗĶČČ£®
×ØĢā£ŗ »Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»Æ£®
·ÖĪö£ŗ A”¢øł¾Ż·ÅČČ·“Ó¦£¬·“Ó¦ĪļµÄ×ÜÄÜĮæŅŖ“óÓŚÉś³ÉĪļµÄ×ÜÄÜĮæĄ“ÅŠ¶Ļ£»
B”¢ÄÜĮæŌ½øßŌ½²»ĪČ¶Ø£¬½įŗĻ·“Ó¦ŹĒ·ÅČČ·“Ó¦£»
C”¢Č¼ÉÕČČĪŖ1molµÄæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪȶØŃõ»ÆĪļ·Å³öµÄČČĮ棻
D”¢0.5 mol H2SO4µÄÅØĮņĖįČܽā¹ż³ĢÖŠ°éĖęČČŠ§Ó¦£®
½ā“š£ŗ ½ā£ŗA”¢Zn£Øs£©+CuSO4£Øaq£©═ZnSO4£Øaq£©+Cu£Øs£©”÷H=﹣216 kJ/mol£¬øł¾Ż”÷H£¼0£¬øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬·“Ó¦ĪļµÄ×ÜÄÜĮæŅŖ“óÓŚÉś³ÉĪļµÄ×ÜÄÜĮ棬¹ŹAÕżČ·£»
B”¢ÄÜĮæŌ½øßŌ½²»ĪČ¶Ø£¬A═B”÷H£¼0£¬ĖµĆ÷AµÄÄÜĮæ±ČBøߣ¬ĖłŅŌA²»ĪČ¶Ø£¬¹ŹB“ķĪó£»
C”¢Č¼ÉÕČČĪŖ1molµÄæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪȶØŃõ»ÆĪļ·Å³öµÄČČĮ棬2molĒāĘų·Å³öµÄČČĮæ“óÓŚ571.6 kJ/mol£¬¹ŹC“ķĪó£»
D”¢0.5 mol H2SO4µÄÅØĮņĖįČܽā¹ż³ĢÖŠ°éĖęČČŠ§Ó¦£¬ĖłŅŌ·Å³öµÄČČĮæ“óÓŚ57.3 kJ£¬¹ŹD“ķĪó£»
¹ŹŃ”A£®
µćĘĄ£ŗ ±¾Ģāæ¼²éĮĖ»Æѧ·“Ó¦ÄÜĮæ±ä»ÆµÄ·ÖĪöÅŠ¶Ļ£¬Ąķ½ā·“Ó¦ČȵÄøÅÄīŹĒ½āĢā¹Ų¼ü£¬ĢāÄæ½Ļ¼ņµ„£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ»ÆѧÓĆÓļÕżČ·µÄŹĒ£Ø£©
A£® F½į¹¹Ź¾ŅāĶ¼ĪŖ£ŗ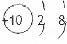
B£® HClµÄµē×ÓŹ½ĪŖ£ŗH+
C£® Na2O2µÄŠĪ³É¹ż³ĢæÉŅŌ±ķŹ¾ĪŖ£ŗ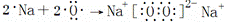
D£® “ĪĀČĖį£ØHClO£©µÄ½į¹¹Ź½ĪŖ£ŗH﹣Cl﹣O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
2HI£Øg£©⇌H2£Øg£©+I2£Øg£©·“Ó¦¹ż³ĢÖŠÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£ØĶ¼ÖŠE1±ķŹ¾Õż·“Ó¦µÄ»ī»ÆÄÜ£¬E2±ķŹ¾Äę·“Ó¦µÄ»ī»ÆÄÜ£©£®ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ£Ø£©
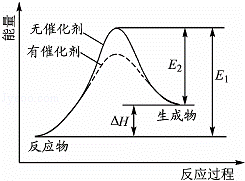
A£® ÉżøßĪĀ¶Č£¬·“Ó¦ĖŁĀŹŌö“󣬔÷H¼õŠ”
B£® ÉżøßĪĀ¶Č£¬²»Ó°Ļģ»ī»Æ·Ö×Ó°Ł·ÖŹż
C£® “߻ƼĮÄܽµµĶøĆ·“Ó¦µÄ»ī»ÆÄÜ
D£® Äę·“Ó¦µÄ»ī»ÆÄܵČÓŚÕż·“Ó¦µÄ»ī»ÆÄÜ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¹ĢĢåNH4BrÖĆÓŚĆܱÕČŻĘ÷ÖŠ£¬Ä³ĪĀ¶ČĻĀ·¢Éś·“Ó¦£ŗNH4Br£Øs£©⇌NH3£Øg£©+HBr£Øg£©£¬2HBr£Øg£©⇌Br2£Øg£©+H2£Øg£©£¬2minŗó²āÖŖH2µÄÅضČĪŖ0.5mol•L﹣1£¬HBrµÄÅضČĪŖ4mol•L﹣1£¬ČōÉĻŹö·“Ó¦ĖŁĀŹÓĆv£ØNH3£©±ķŹ¾£¬ŌņĻĀĮŠĖŁĀŹÕżČ·µÄŹĒ£Ø£©
A£® 0.5mol•L﹣1•min﹣1 B£® 2.5mol•L﹣1•min﹣1
C£® 2mol•L﹣1•min﹣1 D£® 1.25mol•L﹣1•min﹣1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÄÜŌ“Ī£»śŹĒµ±Ē°Č«ĒņĪŹĢā£¬æŖŌ“½ŚĮ÷ŹĒÓ¦¶ŌÄÜŌ“Ī£»śµÄÖŲŅŖ¾Ł“ė£®
£Ø1£©ĻĀĮŠ×ö·ØÓŠÖśÓŚÄÜŌ“”°æŖŌ“½ŚĮ÷”±µÄŹĒ £ØĢī×ÖÄø£©£®
a£®“óĮ¦·¢Õ¹Å©“åÕÓĘų£¬½«·ĻĘśµÄ½ÕøŃ×Ŗ»ÆĪŖĒå½ąøߊ§µÄÄÜŌ“
b£®“óĮ¦æŖ²ÉĆŗ”¢ŹÆÓĶŗĶĢģČ»ĘųŅŌĀś×ćČĖĆĒČÕŅęŌö³¤µÄÄÜŌ“ŠčĒó
c£®æŖ·¢Ģ«ŃōÄÜ”¢Ė®ÄÜ”¢·ēÄÜ”¢µŲČȵȊĀÄÜŌ“£¬¼õÉŁŹ¹ÓĆĆŗ”¢ŹÆÓĶµČ»ÆŹÆČ¼ĮĻ
d£®¼õɣ׏Ō“ĻūŗÄ£¬Ōö¼Ó׏Ō“µÄÖŲø“Ź¹ÓĆ”¢×ŹŌ“µÄŃ»·ŌŁÉś
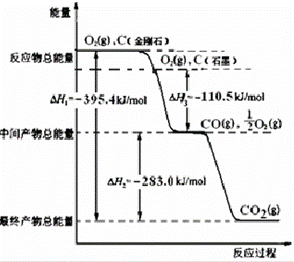
£Ø2£©½šøÕŹÆŗĶŹÆÄ«¾łĪŖĢ¼µÄĶ¬ĖŲŅģŠĪĢ壬ŃõĘų²»×揱ĖüĆĒČ¼ÉÕÉś³ÉŅ»Ńõ»ÆĢ¼£¬³ä·ÖČ¼ÉÕÉś³É¶žŃõ»ÆĢ¼£¬·“Ó¦ÖŠ·Å³öµÄČČĮæČēĶ¼ĖłŹ¾£ŗ
£Øa£©Ķس£×“æöĻĀ£¬½šøÕŹÆŗĶŹÆÄ«ÖŠ £ØĢī”°½šøÕŹÆ”±»ņ”°ŹÆÄ«”±£©øüĪČ¶Ø£¬ŹÆÄ«µÄČ¼ÉÕČČĪŖ”÷H= kJ•mol﹣1£®
£Øb£©12gŹÆÄ«ŌŚŅ»¶ØĮææÕĘųÖŠČ¼ÉÕ£¬Éś³ÉĘųĢå36g£¬ŌņøĆ¹ż³Ģ¹²·Å³öµÄČČĮæ kJ£®
£Ø3£©ŅŃÖŖ£ŗN2£Øg£©+O2£Øg£©=2NO£Øg£©£»”÷H=+180.0kJ•mol﹣1£®×ŪŗĻÉĻŹöÓŠ¹ŲŠÅĻ¢£¬ĒėŠ“³öÓĆCO³żČ„NOµÄČČ»Æѧ·“Ó¦·½³ĢŹ½
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¹ŲÓŚČČ»Æѧ·“Ó¦µÄĆčŹöÖŠÕżČ·µÄŹĒ£Ø£©
A£® HClŗĶNaOH·“Ó¦µÄÖŠŗĶČČ”÷H=﹣5 7.3 kJ/mol£¬ŌņH2SO4ŗĶCa£ØOH£©2·“Ó¦µÄÖŠŗĶČČ”÷H=2”Į£Ø﹣57.3£©kJ/mol
7.3 kJ/mol£¬ŌņH2SO4ŗĶCa£ØOH£©2·“Ó¦µÄÖŠŗĶČČ”÷H=2”Į£Ø﹣57.3£©kJ/mol
B£® Ģ¼Óė¶žŃõ»ÆĢ¼µÄ·“Ó¦¼ČŹĒĪüČČ·“Ó¦£¬ÓÖŹĒ»ÆŗĻ·“Ó¦
C£® ČČ»Æѧ·½³ĢŹ½ÖŠ»Æѧ¼ĘĮæŹżæɱķŹ¾·Ö×ÓøöŹż
D£® 1 mol¼×ĶéČ¼ÉÕÉś³ÉĘųĢ¬Ė®ŗĶ¶žŃõ»ÆĢ¼Ėł·Å³öµÄČČĮæŹĒ¼×ĶéµÄČ¼ÉÕČČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖµØ·ÆČÜÓŚĖ®Ź±ČÜŅŗĪĀ ¶Č½µµĶ£®µØ·Æ·Ö½āµÄČČ»Æѧ·½³ĢŹ½ĪŖCuSO4•5H2O£Øs£©
¶Č½µµĶ£®µØ·Æ·Ö½āµÄČČ»Æѧ·½³ĢŹ½ĪŖCuSO4•5H2O£Øs£© CuSO4£Øs£©+5H2O£Øl£©”÷H=+Q1 mol•L﹣1£®ŹŅĪĀĻĀ£¬Čō½«1molĪŽĖ®ĮņĖįĶČܽāĪŖČÜŅŗŹ±·ÅČČQ2 kJ£¬ŌņQ1ÓėQ2µÄ¹ŲĻµĪŖ£Ø£©
CuSO4£Øs£©+5H2O£Øl£©”÷H=+Q1 mol•L﹣1£®ŹŅĪĀĻĀ£¬Čō½«1molĪŽĖ®ĮņĖįĶČܽāĪŖČÜŅŗŹ±·ÅČČQ2 kJ£¬ŌņQ1ÓėQ2µÄ¹ŲĻµĪŖ£Ø£©
A£® Q1£¾Q2 B£® Q1=Q2 C£® Q1£¼Q2 D£® ĪŽ·Ø±Č½Ļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø£©
A£® ·²ŹĒ·ÅČČ·“Ó¦¶¼ŹĒ×Ō·¢µÄ£¬ÓÉÓŚĪüČČ·“Ó¦¶¼ŹĒ·Ē×Ō·¢µÄ
B£® ×Ō·¢·“Ó¦Ņ»¶ØŹĒģŲŌö“󣬷Ē×Ō·¢·“Ó¦Ņ»¶ØŹĒģŲ¼õÉŁ»ņ²»±ä
C£® ×Ō·¢·“Ó¦ŌŚĒ”µ±Ģõ¼žĻĀ²ÅÄÜŹµĻÖ
D£® ×Ō·¢·“Ó¦ŌŚČĪŗĪĢõ¼žĻĀ¶¼ÄÜŹµĻÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø4£©ĄūÓĆĖ®ĆŗĘųŗĻ³É¶ž¼×ĆѵÄČż²½·“Ó¦ČēĻĀ£ŗ
¢Ł2H2£Øg£©+CO£Øg£©═CH3OH£Øg£©£»”÷H=﹣90.8kJ•mol﹣1
¢Ś2CH3OH£Øg£©═CH3OCH3£Øg£©+H2O£Øg£©£»”÷H=﹣23.5kJ•mol﹣1
¢ŪCO£Øg£©+H2O£Øg£©═CO2£Øg£©+H2£Øg£©£»”÷H=﹣41.3kJ•mol﹣1
×Ü·“Ó¦£ŗ3H2£Øg£©+3CO£Øg£©═CH3OCH3£Øg£©+CO2 £Øg£©µÄ”÷H= £»
Ņ»¶ØĢõ¼žĻĀµÄĆܱÕČŻĘ÷ÖŠ£¬øĆ×Ü·“Ó¦“ļµ½Ę½ŗā£¬ŅŖĢįøßCOµÄ×Ŗ»ÆĀŹ£¬æÉŅŌ²ÉČ”µÄ“ėŹ©ŹĒ £ØĢī×ÖÄø“śŗÅ£©£®
a£®øßĪĀøßŃ¹ b£®¼ÓČė“߻ƼĮ c£®¼õÉŁCO2µÄÅØ¶Č d£®Ōö¼ÓCOµÄÅضČe£®·ÖĄė³ö¶ž¼×ĆŃ£®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com