
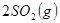
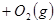

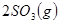 从正方向开始,并达到了平衡,此时
从正方向开始,并达到了平衡,此时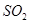 和
和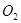 的物质的量之比为2:1,若采取某种措施,导致
的物质的量之比为2:1,若采取某种措施,导致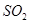 和
和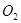 又消耗了一些,并再次达到平衡,下列说法正确的是
又消耗了一些,并再次达到平衡,下列说法正确的是A.新平衡体系中,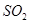 和 和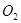 物质的量之比仍为2:1 物质的量之比仍为2:1 |
| B.平衡向正反应方向移动,原因是正反应速率增大,逆反应速率减小 |
C.新平衡体系与旧平衡体系比较,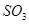 的浓度肯定增大 的浓度肯定增大 |
D.若所采取的措施是缩小容器的容积,则新旧平衡中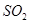 和 和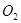 的转化率之比都是1:1 的转化率之比都是1:1 |
科目:高中化学 来源:不详 题型:填空题
 N2O4(g)达到平衡。其他条件不变时,下列措施能提高NO2转化率的是 (填字母)。
N2O4(g)达到平衡。其他条件不变时,下列措施能提高NO2转化率的是 (填字母)。| A.减小NO2的浓度 | B.降低温度 |
| C.增加NO2的浓度 | D.升高温度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g) △H<0,下列研究目的与示意图相符的是
2NH3(g) △H<0,下列研究目的与示意图相符的是| | A | B | C | D |
| 研究目的 | 压强对反应的影响(P2<P1) | 温度对反应的影响 | 恒温恒容时,向平衡中增加N2对反应的影响 | 催化剂对反应的影响 |
| 图示 | 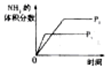 | 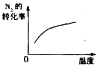 | 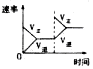 | 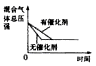 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
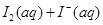

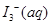
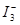 的物质的量浓度c(
的物质的量浓度c(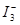 )与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是
)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是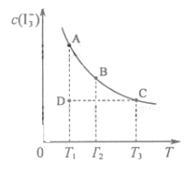
A.反应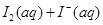  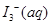 △H>0[ △H>0[ |
B.若温度为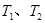 ,反应的平衡常数分别为 ,反应的平衡常数分别为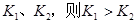 |
C.若反应进行到状态D时,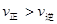 |
| D.状态A与状态B相比,状态A的c(I2)大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2A(g)+B(g) 2C(g) △H<0,4s后反应达到平衡状态,此时测得C的浓度为0.6mol·L-1,下列说法中正确的是 ( )
2A(g)+B(g) 2C(g) △H<0,4s后反应达到平衡状态,此时测得C的浓度为0.6mol·L-1,下列说法中正确的是 ( )| A.当容器内混合气体的密度不再发生变化时,反应即达到平衡状态 |
| B.达平衡后若升高温度,该反应的平衡常数将增大 |
| C.平衡时反应物B的转化率为15.0% |
| D.达平衡后,如果此时移走2molA和1molB,在相同温度下再达平衡时C的浓度<0.3mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.已知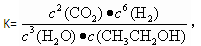 则对应的化学反应可以表示为: 则对应的化学反应可以表示为:2CO2(g) + 6H2(g) 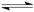 CH3CH2OH(g) + 3H2O(g) CH3CH2OH(g) + 3H2O(g) |
| B.将某浓度醋酸溶液升高温度,醋酸的电离平衡常数Ka将变大 |
| C.常温下,向纯水中加入少量碳酸钠固体,水的电离程度变大,Kw变大 |
D.常温下,在饱和氯水中加入少量碳酸钙固体,Cl2+H2O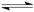 HCl+HClO平衡正移,平衡常数K变大 HCl+HClO平衡正移,平衡常数K变大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
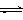 CH3OH(g)+H2O(g) △H=—49kJ/mol,测得CO2和H2O (g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) △H=—49kJ/mol,测得CO2和H2O (g)的浓度随时间变化如图所示。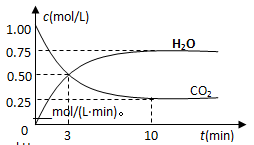
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
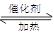 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L 。
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L 。 2SO3(g) ΔH =" -" 196.6 kJ· mol-1
2SO3(g) ΔH =" -" 196.6 kJ· mol-1 2NO2(g) ΔH =" -" 113.0 kJ· mol-1
2NO2(g) ΔH =" -" 113.0 kJ· mol-1 SO3(g)+NO(g)的ΔH = kJ· mol-1。
SO3(g)+NO(g)的ΔH = kJ· mol-1。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com