
| A. | 甲-②,乙-④ | B. | 乙-③,丙-③ | C. | 乙-④,丁-② | D. | 丙-①,丁-② |
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol过氧化氢完全分解转移的电子数目为0.4NA | |
| B. | 300 mL 2 mol/L蔗糖溶液中所含分子数为0.6 NA | |
| C. | 在常温常压下,17 g硫化氢所含质子数目为8 NA | |
| D. | 在标准状况下,2.24 L二氧化硫与氧气混合气体中所含氧原子数为0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L二氯甲烷的分子数约为NA | |
| B. | 室温下,1L pH=12的碳酸钠溶液中含有Na+的数目为0.02NA | |
| C. | 1L 0.1mol•L-1K2Cr2O7溶液中Cr2O72-的数目小于0.1NA | |
| D. | 电解精炼铜时,若阴极得到的电子数为2NA,则阳极质量一定减少64 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
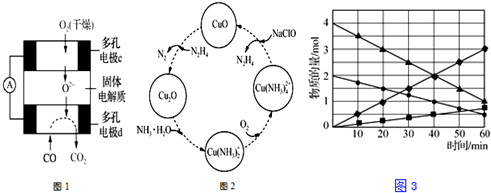
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Zn与浓硫酸反应可获得高浓度SO2 | |
| B. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 | |
| C. | 选择相同的气体发生装置分别用Na2O2、CaCO3制备O2、CO2 | |
| D. | 可用分液的方法分离碘和酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C、N、O三种元素的氢化物稳定性依次减弱 | |
| B. | Mg、Al、Si三种元素的原子半径依次减小 | |
| C. | F、Cl、Br三种元素的非金属性依次减弱 | |
| D. | Li、Na、K三种元素的最高价氧化物对应水化物碱性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其保持平衡,然后向左侧烧杯中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(不考虑两球的浮力变化)( )
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其保持平衡,然后向左侧烧杯中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(不考虑两球的浮力变化)( )| A. | 杠杆为导体或绝缘体时,均为A端高B端低 | |
| B. | 杠杆为导体或绝缘体时,均为A端低B端高 | |
| C. | 当杠杆为导体时,A端高B端低 | |
| D. | 当杠杆为导体时,A端低B端高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| B. | 萃取碘水中碘,用无毒无害的酒精代替四氯化碳更加环保 | |
| C. | 不可以用过滤的方法除去粗盐中的CaCl2、MgCl2等杂质 | |
| D. | 用丁达尔效应区分FeCl3溶液和Fe(OH)3胶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com