
【题目】化学电池在通讯、交通及日常生活中有着广泛的应用.目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:Cd+2NiO(OH)+2H2O![]() 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法正确的是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法正确的是
①以上反应是可逆反应 ②以上反应不是可逆反应
③Cd为电池的正极 ④放电时化学能转变为电能.
A.①③B.②④C.①④D.②③
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】Prolitane 是一种抗抑郁药物,以芳香烃 A 为原料的合成路线如下:

请回答以下问题:
(1)A 的结构简式为_____。D 的化学名称为_____,
(2)E 的官能团名称分别为_____和_____。
(3)H→Prolitane 的反应类型为_____。
(4)F→G 的化学方程式为_____。
(5)C 的同分异构体中能同时满足下列条件的共有_____种(不含立体异构);
①属于芳香化合物
②能发生银镜反应
③能发生水解反应
其中核磁共振氢谱显示为 4 组峰,其峰面积比为 3∶2∶2∶1,写出符合要求的该同分异构体的结构简式_____________。
(6)参照 Prolitane 的合成路线,设计一条由苯和乙醇为原料制备苯甲酸乙酯的合成路线(其他无机试剂和溶剂任选):__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲乙两装置的电极材料和电解质溶液均相同,则两装置中相同的是( )

A.在碳电极上所发生的电极反应B.在铁电极附近的溶液先变红色
C.铁极与导线连接处的电流方向D.碳电极既不会变大也不会减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、S 的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1)CO2 的重整用 CO2 和 H2 为原料可得到 CH4 燃料。
已知: ①CH4 (g)+CO2(g)=2CO(g)+2H2(g) △H1=+247kJ/mol
②CH4 (g)+H2O(g)=CO(g)+3H2(g) △H2=+205kJ/mol
写出 CO2 重整的热化学方程式:_____。
(2) “亚碳酸盐法”吸收烟中的 SO2
①将烟气通入 1.0mol/L 的 Na2SO3 溶液,若此过程中溶液体积不变,则溶液的 pH 不断_____(填“减小”“不变” 或“增大)。当溶液 pH 约为 6 时,吸收 SO2 的能力显著下降,应更换吸收剂,此时溶液中 c(SO32-) =0.2mol/L, 则溶液中 c(HSO3-) =_____。
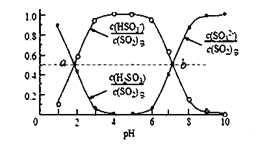
②室温条件下,将烟气通入(NH4)2SO3 溶液中,测得溶液 pH 与各组分物质的量分数的变化关系如图: b 点时溶液 pH=7,则 n(NH4+):n(HSO3—)= ______________ 。
(3)催化氧化法去除 NO。一定条件下,用 NH3 消除 NO 污染,其反应原理4NH3+6NO![]() 5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为 4:1、3:1、1:3 时,得到 NO 脱除率曲线如图所示:
5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为 4:1、3:1、1:3 时,得到 NO 脱除率曲线如图所示:
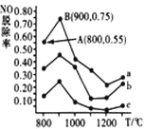
①曲线 a 中,NO 的起始浓度为6×10-4mg·m-3,从 A 点到 B 点经过0.8s,该时间段内 NO 的脱除速率为_____mg·m-3·s-1。
②曲线 b 对应 NH3 与 NO 的物质的量之比是_____。
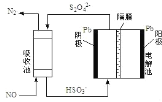
(4)间接电化学法除 NO。其原理如图所示:写出阴极的电极反应式(阴极室溶液呈酸性)_____。吸收池中除去 NO 的原理_____(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器内,使1molN2和3molH2混合发生下列反应:3H2+N2![]() 2NH3△H<0。
2NH3△H<0。
(1)合成氨时选择500℃高温的目的是______________。
(2)当反应达到平衡时,N2和H2的浓度比是_______。
(3)当达到平衡吋,充入氩气,并保持体积不变,平衡将______移动。
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将______移动,反应速率将_______。
(5)当达到平衡时,充入N2并保持体积不变,平衡将______移动。
(6)当达到平衡时,保持体积不变,升高温度时,混合气体的平均相对分子质量_______(选填“增大”“减小”或“不变”,后同),密度________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是 ( )
A. 向水中通入氯气:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B. 向氯化铁溶液中加入铜:2Fe3++3Cu===2Fe+3Cu2+
C. NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
D. 向二氧化锰中滴加浓盐酸并加热:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫、氯的单质和化合物应用广泛。
(1)将硫铁矿和焦炭按物质的量之比为3∶2混合放在炼硫炉中,通入适量空气,发生下列燃烧反应:
FeS2+C+O2→Fe3O4+CO+S。
配平上述化学反应方程式:______________________________。生成3 mol硫,被氧化物质的物质的量为__________________。
(2)盐酸是应用广泛的酸之一,它具有
a.酸性;b.氧化性;c.还原性;d.挥发性。
请回答下列问题:
①浓盐酸长时间露置在空气中,溶液的质量减轻,盐酸表现了________(填序号)。
②实验室用稀盐酸和锌粒反应制取氢气,盐酸表现了________(填序号),反应的离子方程式为_____________________________________________________________________。
③用盐酸除去铁表面的铁锈,盐酸表现了______(填序号),反应的离子方程式为__________________________________________________________________。
④实验室常用KMnO4和浓盐酸反应制取Cl2,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。被还原的元素是______,还原剂是______,氧化产物是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,三种酸的电离平衡常数如下表所示。
化学式 | CH3COOH | HClO | H3PO3 |
名称 | 醋酸 | 次氯酸 | 亚磷酸 |
电离平衡常数 | 1.8×10-5 | 3.0×10-8 | K1=8.3×10-3 K2 =5.6×10-6 |
回答下列问题:
(1)浓度均为0.1 molL-1的CH3COOH 、HClO 、H3PO3溶液中,c(H+)最小的是_____________。
(2)亚磷酸(H3PO3)为二元酸,具有较强的还原性。H3PO3的第二级电离方程式为________________。Na2HPO3是_____________(填“酸式盐”“碱式盐”或“正盐”)。
(3)常温下,0.1 molL-1的CH3COOH溶液加水稀释的过程中,下列表达式的数值变大的是______(填字母)。
A.c(H+) B. 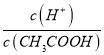 C.c(CH3COO-) D.c(CH3COOH)
C.c(CH3COO-) D.c(CH3COOH)
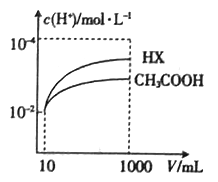
(4)体积均为10mL、c(H+)均为10-2 mol L-1的醋酸溶液与一元酸HX分别加水稀释至1000 mL,稀释过程中c(H+)的变化如图所示,则HX的电离平衡常数_______________(填“大于”“ 小于”或“等于”)醋酸的电离平衡常数,理由是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的相关表述中正确的是
A. 因H+(aq) +OH- (aq)==H2O(l) △H=-akJ·mol-1,故1molNaOH固体与足量的稀盐酸反应,放出的热量为akJ
B. 因CuSO4·5H2O(s)==CuSO4(s)+5H2O(1)△H=+bkJ·mol-1,故1molCuSO4(s)溶于水时,放出的热量为bkJ
C. 因氢气的燃烧热为c kJ·mol-1,故水电解的热化学方程式为2H2O (l)==2H2(g)+O2(g) △H=+c kJ·mol-1
D. 因N2(g)+3H2(g)![]() 2NH3(g) △H=-d kJ·mol-1,故在某容器中通入1molN2与3molH2充分反应后,放出的热量小于dkJ
2NH3(g) △H=-d kJ·mol-1,故在某容器中通入1molN2与3molH2充分反应后,放出的热量小于dkJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com