
| A. | 硫酸盐 | B. | 铵盐 | C. | 正盐 | D. | 酸式盐 |
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂和还原剂的物质的量之比为1:14 | |
| B. | 由该反应可知还原性:HCl>CrCl3 | |
| C. | 当转移0.2mol电子时,被氧化的还原剂的物质的量为0.2mol | |
| D. | Cl2是该反应的氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
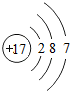 ;
; ,该化合物的水溶液在空气中久置后变质,生成一种单质和一种强碱,用化学方程式表示这一变化过程并用单线桥标记电子转移的方向和数目:
,该化合物的水溶液在空气中久置后变质,生成一种单质和一种强碱,用化学方程式表示这一变化过程并用单线桥标记电子转移的方向和数目: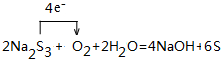
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应 | A | B | C | D |
| △H/(kJ•mol-1) | 10.5 | 1.80 | -126 | -11.7 |
| △S/(J•mol-1•k-1) | 30.0 | -113.0 | 84.0 | -105.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3(12e-) | B. | NOx(12e-) | C. | NH3(12xe-) | D. | NOx(12xe-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=-98.3KJ•mol-1 | |
| B. | 2SO2(g)+O2(g)?2SO3(l);△H=-196.6KJ•mol-1 | |
| C. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=-78.64KJ•mol-1 | |
| D. | 2SO2(g)+O2(g)?2SO3(g);△H=+196.6KJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加酸性高锰酸溶液,振荡 | B. | 加NaOH溶液,煮沸 | ||
| C. | 加新制Cu(OH)2悬浊液,煮沸 | D. | 加溴水,振荡 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com