
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入硝酸银,产生白色沉淀,再加稀硝酸,沉淀不溶解,则溶液中一定有Cl- | |
| D. | 加入KSCN,溶液变血红色,则溶液中一定有Fe2+ |
分析 A.盐酸能与含碳酸根或碳酸氢根离子的物质反应生成二氧化碳,二氧化碳气体遇澄清石灰水变浑浊;
B.氯化钡能与硫酸根离子或银离子结合生成不溶于水也不溶于酸的沉淀;
C.加入硝酸银生成的不溶于硝酸的沉淀为氯化银,则溶液中含有氯离子;
D.亚铁离子不与硫氰根离子反应,铁离子与硫氰根离子反应,溶液变红色.
解答 解:A.盐酸能与含碳酸根或碳酸氢根离子的物质反应生成二氧化碳,加入稀盐酸产生无色气体,原溶液中可能含有碳酸氢根离子,不一定有CO32-,故A错误;
B.氯化钡能与硫酸根离子或银离子结合生成不溶于水也不溶于酸的沉淀,加入氯化钡溶液有白色沉淀产生,该沉淀可能为氯化银,溶液中不一定含有硫酸根离子,故B错误;
C.加入硝酸银,产生白色沉淀,再加稀硝酸,沉淀不溶解,该沉淀为氯化银,说明溶液中一定有Cl-,故C正确;
D.KSCN,溶液变血红色,则溶液中一定有Fe3+,不能确定是否含有亚铁离子,故D错误;
故选C.
点评 本题考查了常见离子的检验方法,题目难度中等,注意掌握常见离子的性质及检验方法,明确检验离子存在时,必须排除干扰离子,确保检验方案的严密性.


科目:高中化学 来源: 题型:选择题
| A. | 在1 mol•L-1的KClO3溶液中,K+的个数为NA | |
| B. | 在标准状况下,22.4 L CH3CH2OH的分子数为NA | |
| C. | 32 g氧气和臭氧的混和气体中含有的氧原子数为2NA | |
| D. | 22.4 L HCl气体中含有的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化氢的电子式为 H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$]- | |
| B. | 乙炔的结构简式(删:可以)写成 CHCH | |
| C. | 镁的原子结构示意图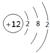 | |
| D. | 碳酸氢钠溶于水电离方程式:NaHCO3═Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 45 | B. | 25 | C. | 29 | D. | 39 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,BN中B元素的化合价为+3;
,BN中B元素的化合价为+3; ,其二氯代物有4种.
,其二氯代物有4种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/10-10m | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 1.43 |
| 最高化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低化合价 | -2 | -3 | -1 | -3 |
| A. | 元素③与⑧的金属性相比:前者强于后者 | |
| B. | 上述8种元素中,元素⑤的最高价氧化物对应的水化物酸性最强 | |
| C. | 元素⑦的气态氢化物与元素④的气态氢化物相比较:前者稳定性强,后者沸点高 | |
| D. | 元素①分别与元素②和⑥形成的化合物所含化学键类型不一定完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
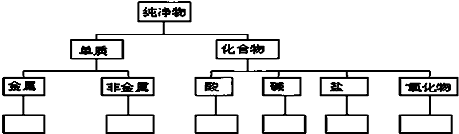
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com