
| A. | 原子半径:Se>S | B. | 沸点:H2S>H2Se | ||
| C. | 稳定性:H2S>H2Se | D. | 酸性:H2SO4>H2SeO4 |
分析 同主族从上到下,元素的非金属性减弱、氢化物的稳定性减弱、最高价含氧酸的酸性减弱、原子半径增大,氢化物的沸点升高,据此分析.
解答 解:A.同主族从上到下,原子半径增大,则原子半径:Se>S,故A正确;
B.氢化物的相对分子质量越大,沸点越高,则沸点:H2S<H2Se,故B错误;
C.同主族从上到下,元素的非金属性减弱、氢化物的稳定性减弱,则H2S>H2Se,故C正确;
D.同主族从上到下,元素的非金属性减弱,最高价含氧酸的酸性减弱,则酸性:H2SO4>H2SeO4,故D正确.
故选B.
点评 本题考查元素及化合物的性质,把握同主族元素性质的相似性和递变性为解答的关键,本题注意利用类推的方法思考,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 原子半径:r(W)>r(Y)>r(Z)>r(X) | |
| B. | X、Y、Z三种元素形成的化合物中只有共价键 | |
| C. | 最高价氧化物对应水化物的酸性:W>Y | |
| D. | 气态简单氢化物的热稳定性:Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用NH3表示反应①的速率为1 mol/(L•min) | |
| B. | 体系中颜色不再变化时,可判断反应均已达平衡 | |
| C. | 该温度下反应①的平衡常数为20 mol2/L2 | |
| D. | 加压时反应②的平衡不会移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)=c(H2PO4-)+c(HPO42-)+C(H3PO4) | |
| B. | c(Na+)+c(H+)=c(OH-)+c(H2PO4-)+2c(HPO42-)+3c(PO43-) | |
| C. | 温度升高,c(H2PO4-)增大 | |
| D. | 加水稀释后,m(H+)与m(OH-)的乘积不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用铝热反应焊接钢轨:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 2Fe+Al2O3 | |
| B. | 用氯水除去FeCl3溶液中的Fe2+:Cl2+Fe2+═2Cl-+Fe3+ | |
| C. | 用已知浓度的NaOH溶液测定未知浓度的醋酸溶液的浓度:H++OH-═H2O | |
| D. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2Na++2OH-═Na2SiO3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
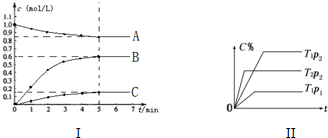
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 多氯代甲烷中分子结构为正四面体的是二氯甲烷和四氯化碳 | |
| B. | 多氯代烷常为有机溶剂,工业上分离这些多氯代物的方法是萃取 | |
| C. | 三氟氯溴乙烯(CF3CHClBr)是一种麻醉剂,有4种同分异构体(不考虑立体异构) | |
| D. | 聚氯乙烯是生活中常用的塑料,工业上以乙烯为原料经过加成、消去和聚合反应可生成聚氯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100g98%的浓H2SO4中所含的氧原子数为4NA(NA为阿伏伽德罗常数,下同) | |
| B. | 3.1g白磷晶体中含有的P-P键数是0.6NA | |
| C. | 向Ca(HCO3)2溶液中加入Ca(OH)2溶液至过量:Ca2++2HCO3-+2OH-═CaCO3↓+CO${\;}_{3}^{2-}$+2H2O | |
| D. | 冰水中常会形成(H2O)x(x≥1)分子,原因是存在氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 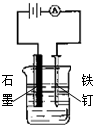 装置:防止铁钉生锈 | B. |  装置:可制得金属锰 | ||
| C. |  装置:实验室制取乙酸乙酯 | D. | 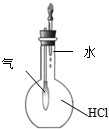 装置:验证HCl气体在水中的溶解性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com