
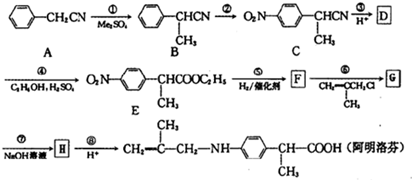
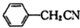 ,对称结构,核磁共振氢谱中有4种峰;
,对称结构,核磁共振氢谱中有4种峰;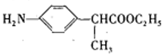 ,F与
,F与 发生取代反应生成G,G在碱性条件下发生水解反应生成H,所以H为
发生取代反应生成G,G在碱性条件下发生水解反应生成H,所以H为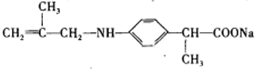 ;
; .
. ,对称结构,核磁共振氢谱中有4种峰,故答案为:4;
,对称结构,核磁共振氢谱中有4种峰,故答案为:4; ,F与
,F与 发生取代反应生成G,G在碱性条件下发生水解反应生成H,所以H为
发生取代反应生成G,G在碱性条件下发生水解反应生成H,所以H为 ,故答案为:
,故答案为: ;
; ;
; ,
, ;
;


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
| A、200 mL 0.1 mol/L NH4Cl 溶液 |
| B、50 mL 0.2 mol/L NH4NO3溶液 |
| C、100 mL 0.2 mol/L NH4HSO4 |
| D、50 mL 0.2 mol/L氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、320g | B、160g |
| C、64g | D、32g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、126C、136C、146C 为碳元素的三种核素.元素周期表中碳的相对原子质量为12.01,说明自然界中的碳主要以126C 的核素形式存在.146C为放射性核素,可用于同位素示踪 |
| B、汽车尾气催化转化装置可将尾气中的NO和CO等有害气体转化为N2和CO2,该装置中的催化剂可降低NO和CO反应的活化能,有利于提高该反应的平衡转化率 |
| C、道尔顿、汤姆生、卢瑟福、玻尔等科学家的研究不断更新人们对原子结构的认识 |
| D、地沟油由于混有一些对人体有害的杂质而不能食用,可加工制成生物柴油,生物柴油的成分与从石油中提取的柴油成分不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
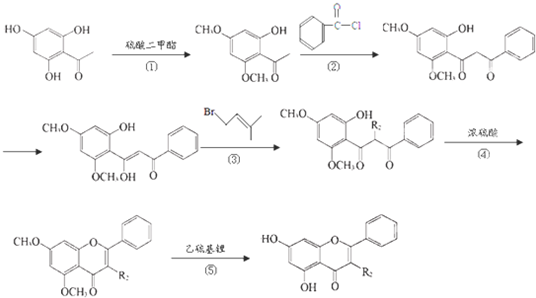
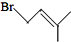 的同分异构体有
的同分异构体有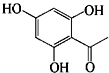 说法正确的是
说法正确的是查看答案和解析>>
科目:高中化学 来源: 题型:

| 红磷 |
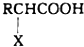 +HX
+HX查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨气是非电解质,氨水是电解质 |
| B、氢氧化铁胶体可以发生丁达尔现象 |
| C、摩尔和物质的量均是联系宏观和微观数量的物理量 |
| D、二氧化硅既可和酸又可和碱反应,所以二氧化硅是两性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
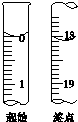 Na2SO3因易被氧化成Na2SO4而变质,某化学兴趣小组为了测定实验室存放的Na2SO3的纯度(假设不含其它杂质),进行如下实验.
Na2SO3因易被氧化成Na2SO4而变质,某化学兴趣小组为了测定实验室存放的Na2SO3的纯度(假设不含其它杂质),进行如下实验.查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、CuO作还原剂 |
| B、CO作氧化剂 |
| C、铜元素的化合价降低 |
| D、碳元素的化合价降低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com