
| A、分离NaCl和SiO2 |
| B、.从溶液中蒸发得到晶体 |
| C、.分离酒精和水 |
| D、.分离汽油和水 |


科目:高中化学 来源: 题型:
| 化学键 | Si-O | O═O | Si-Si |
| 键能/kJ?mol-1 | X | 498.8 | 176 |
| A、423.3 | B、460 |
| C、832 | D、920 |
查看答案和解析>>
科目:高中化学 来源: 题型:

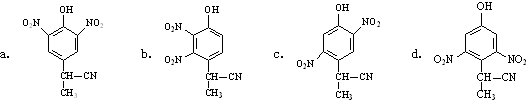
 为原料制备
为原料制备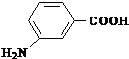 的合成路线流程图(无机试剂任选).合成路线流程图示例如图:CH2=CH2
的合成路线流程图(无机试剂任选).合成路线流程图示例如图:CH2=CH2| HBr |
| 催化剂,△ |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| I1 | I2 | I3 | I4 | … | |
| R | 740 | 1 500 | 7 700 | 10 500 | … |
| A、R的最高正价为+3价 |
| B、R元素位于元素周期表中第ⅡA族 |
| C、R元素的原子最外层共有4个电子 |
| D、R元素基态原子的电子排布式为1s22s22p1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题:
化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题:2- 4 |
| H+ |
| 转化 |
2- 7 |
| Fe2+ |
| 还原 |
| CH- |
| 沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com