
| A. | NaBH4与盐酸不反应 | |
| B. | NaBH4的电子式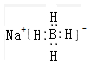 | |
| C. | 每生成1molFe,转移2mol电子 | |
| D. | 氧化产物与还原产物的物质的量之比为1:1 |
分析 反应2FeSO4+NaBH4+4NaOH=2Fe+2H2↑+Na[B(OH)4]+2Na2SO4中,FeSO4中的Fe由+2降低到0价,生成2Fe为还原产物,NaBH4中H元素由-1价升高到0价,生成2H2为氧化产物,以此解答该题.
解答 解:A.由反应2FeSO4+NaBH4+4NaOH=2Fe+2H2↑+Na[B(OH)4]+2Na2SO4中,NaBH4中H元素由-1价升高到0价,则NaBH4具有还原性,所以与盐酸发生归中反应生成氢气,故A错误;
B.NaBH4为离子化合物,则电子式为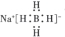 ,故B正确;
,故B正确;
C.反应2FeSO4+NaBH4+4NaOH=2Fe+2H2↑+Na[B(OH)4]+2Na2SO4中,FeSO4中的Fe由+2降低到0价,所以每生成1molFe,转移2mol电子,故C正确;
D.反应2FeSO4+NaBH4+4NaOH=2Fe+2H2↑+Na[B(OH)4]+2Na2SO4中,FeSO4中的Fe由+2降低到0价,则生成2Fe为还原产物,NaBH4中H元素由-1价升高到0价,则生成2H2为氧化产物,所以氧化产物与还原产物的物质的量之比为1:1,故D正确;
故选A.
点评 本题考查氧化还原反应中的有关概念和电子转移知识,为高频考点,侧重于基本概念的理解和运用的考查,注意从化合价的角度解答该题,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 平衡向正反应方向移动 | B. | 平衡将向逆反应方向移动 | ||
| C. | 平衡不发生移动 | D. | 容器内气体的密度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间/min | n(A)mol | n(C)mol |
| 0 | 0.3 | 0 |
| 1 | 0.15 | 0.15 |
| 2 | 0.1 | 0.2 |
| 3 | 0.1 | 0.2 |
| A. | x=1 | |
| B. | 反应开始2min内,用B表示的反应速率为0.05mol•L-l•min -1 | |
| C. | 反应进行到lmin时,反应体系达到化学平衡状态 | |
| D. | A的正反应速率等于C的逆反应速率时,反应体系达到化学平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠熔化时离子键被破坏 | |
| B. | 二氧化硅融化和干冰气化所破坏的作用力不相同 | |
| C. | H2SO4、CCl4、NH3均属于共价化合物 | |
| D. | HBr比HCl的热稳定性差说明HBr的分子间作用力比HCl弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向碳酸氢钠溶液中滴加氢氧化钠溶液:OH-+HCO3-═CO32-+H2O | |
| B. | 溴化亚铁溶液中通入足量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+2Cl- | |
| C. | 工业上将硫酸工业尾气SO2持续通入氨水中SO2+OH-═HSO3- | |
| D. | 向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.1 mol•L-1 NH4Cl溶液的pH=1 | |
| B. | 工业上电解饱和食盐水时,以石墨为阴极,铁棒为阳极 | |
| C. | 反应CO2(g)+C(s)═2CO(g)在高温下可自发进行,则该反应的△H>0 | |
| D. | 常温下,在AgCl悬浊液中加入少量NaCl饱和溶液,[Ag+]减小,Ksp(AgCl)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃煤时加适量的生石灰可减少二氧化硫的排放 | |
| B. | pH在5.6~7.0之间的降水通常称为酸雨 | |
| C. | 焚烧一次性饭盒可减少白色污染 | |
| D. | 实验室可用氢氧化钠溶液除去尾气中的NO气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com