
| A. | 0.5mol/LNaHSO4与0.5mol/LBa(OH)2混合至溶液呈中性:Ba2++OH-+SO42-+H+═BaSO4↓+H2O | |
| B. | 向2mol/LFe(NO3)2(aq)中滴加少量氢碘酸:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O | |
| C. | 向20mL0.5mol/LFeBr2(aq)中通入224mLCl2(标况):2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| D. | 向30mL0.5mol/LNaOH(aq)中通入224mLCO2(标况):3OH-+2CO2═CO32-+HCO3-+H2O |
分析 A.NaHSO4溶液与Ba(OH)2溶液反应至中性,二者的物质的量之比为2:1;
B.硝酸根离子氧化碘离子;
C.n(FeBr2)=0.01mol,n(Cl2)=0.01mol,氯气不足,氧化部分Br-;
D.n(NaOH)=0.015mol,n(CO2)=0.01mol,二者按照3:2的比值反应.
解答 解:A.NaHSO4溶液与Ba(OH)2溶液反应至中性,二者的物质的量之比为2:1,离子反应为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故A错误;
B.向2mol/LFe(NO3)2(aq)中滴加少量氢碘酸,首先氧化电离子,反应的离子方程式为6I-+2NO3-+8H+═3I2+2NO↑+4H2O,故B错误;
C.n(FeBr2)=0.01mol,n(Cl2)=0.01mol,氯气不足,氧化部分Br-,反应的离子方程式为2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl-,故C错误;
D.n(NaOH)=0.015mol,n(CO2)=0.01mol,二者按照3:2的比值反应,反应的离子方程式为3OH-+2CO2═CO32-+HCO3-+H2O,故D正确.
故选D.
点评 本题考查了离子方程式的正误判断,题目难度中等,试题侧重于元素化合物的性质的综合应用,注意物质的化学式、电荷守恒和质量守恒的判断.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 性状 | 熔点/℃ | 沸点/℃ | 水溶性 | |
| N2H4 | 无色液体 | 1.4 | 113 | 与水混溶 |
| N2H6SO4 | 无色晶体 | 254 | / | 微溶于冷水,易溶于热水 |
| 步骤 | 操作 | 现象 |
| I | 取10g NaClO固体,加入100mL水 | 固体溶解,溶液呈碱性 |
| II |  | 液面上方出现白雾 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
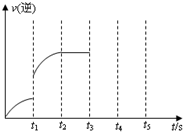 一定温度下在体积为5L的密闭容器中发生可逆反应.
一定温度下在体积为5L的密闭容器中发生可逆反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水鉴别乙醇、苯和四氯化碳 | |
| B. | 用饱和硫酸铵溶液可分离淀粉和蛋白质的混合溶液 | |
| C. | 用碳酸钠溶液可鉴别乙醇、乙酸和乙酸乙酯 | |
| D. | 用酸性高锰酸钾溶液鉴别苯、植物油和裂化汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 特氟隆(聚四氟乙烯)的单体是氟利昂 | |
| B. | 蛋白质是由氨基酸形成的可水解的高分子化合物,其水溶液有丁达尔现象 | |
| C. | 聚丙烯的结构简式为: | |
| D. | 石英的化学式为CaSiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有碳酸根离子 | |
| B. | 加入氯化钡溶液有白色沉淀生成,再加盐酸,沉淀不消失,一定有硫酸根离子 | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有氨根离子 | |
| D. | 为检验酸性溶液中的氯离子和硫酸根离子,应先加硝酸银溶液,滤去沉淀后加硝酸钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{8}^{16}$O、${\;}_{8}^{18}$O为不同的核素,有不同的化学性质 | |
| B. | H2、SO2、NH3三种气体都可用浓硫酸干燥 | |
| C. | 分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 | |
| D. | 陶瓷、玻璃、水泥、大理石的主要成分都是硅酸盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com