
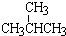 和
和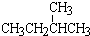 ; ②
; ②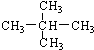 和
和 ; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).
; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).| 类别 | 同位素 | 同系物 | 同素异形体 | 同分异构体 |
| 组号 | ⑤⑥ | ①③ | ④⑧ | ②⑦ |
分析 根据同位素、同系物、同素异形体、同分异构体的概念判断,若化学式为元素,可能是同位素;若化学式为单质,则可能是同素异形体;若化学式为分子式相同、结构不同的有机化合物,则为同分异构体;若是分子式不同结构相似的有机化合物,则为同系物.
解答 解:若化学式为元素,可能是同位素;若化学式为单质,则可能是同素异形体;若化学式为分子式相同、结构不同的有机化合物,则为同分异构体;若是分子式不同结构相似的有机化合物,则为同系物.
所以①结构相似,分子组成相差1个“CH2”原子团,互为同系物; ②分子式都为C5H12相同,但结构不同,互为同分异构体;③结构相似,分子组成相差2个“CH2”原子团,互为同系物;④金刚石与石墨都是由碳元素形成的不同单质,互为同素异形体;⑤氕、氘与氚的质子数相同,中子数不同,故互为同位素;⑥16O、17O和18O的质子数相同,中子数不同,故互为同位素;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3)分子式相同,但结构不同,互为同分异构体;⑧氧气(O2)与臭氧(O3)都是由氧元素形成的不同单质,互为同素异形体;根据以上分析可知,互为同位素的为:⑤⑥,互为同系物的为:①③;互为同素异形体的为:④⑧;互为同分异构体的为:②⑦,
故答案为:
| 类别 | 同位素 | 同系物 | 同素异形体 | 同分异构体 |
| 组号 | ⑤⑥ | ①③ | ④⑧ | ②⑦ |
点评 本题考查了同位素、同系物、同素异形体、同分异构体的概念判断,判断同位素、同素异形体、同分异构体的方法是:是元素的可能是同位素;是单质的可能是同素异形体;分子式相同、结构不同的为同分异构体,题目难度不大.


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:选择题

| A. | 元素Y与元素Z的最高正化合价之和的数值等于9 | |
| B. | 原子半径的大小顺序为:W>Z>Y | |
| C. | 离子半径的大小顺序为:W2->Y2->Z3+ | |
| D. | W的气态氢化物的热稳定性和还原性均比Q的氢化物的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30g二氧化硅晶体中含有Si-O键数目为2NA | |
| B. | 标准状况下,2.24L CHCl3的原子总数为0.1NA | |
| C. | 一定条件下,将1molN2与3molH2混合反应后,生成NH3分子的数目为2NA | |
| D. | 常温下,0.1mol/LNH4NO3溶液NO${\;}_{3}^{-}$的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
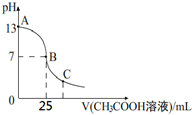 25℃时,向25mL 一定浓度的 NaOH溶液中逐滴加入某浓度的 CH3COOH溶液,溶液pH和加入的醋酸溶液的体积关系曲线如图所示.下列有关混合溶液说法错误的是( )
25℃时,向25mL 一定浓度的 NaOH溶液中逐滴加入某浓度的 CH3COOH溶液,溶液pH和加入的醋酸溶液的体积关系曲线如图所示.下列有关混合溶液说法错误的是( )| A. | A、B间的溶液中可能有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | B点:c(CH3COO-)=c(Na+)>c(OH-)=c(H+) | |
| C. | C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| D. | NaOH溶液和醋酸溶液的浓度都恰好为0.1 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向碘化钾溶液中加入用硫酸酸化的过氧化氢溶液:2I-+H2O2═I2+2OH- | |
| B. | 向碳酸氢铵溶液中加入过量的稀氢氧化钠溶液:NH4++HCO3-+2OH-═NH3•H2O+CO32-+H2O | |
| C. | 向Ba(OH)2溶液中加入过量NH4HSO4:Ba2++H++NH4++2OH-+SO 42-═BaSO4↓+H2O+NH3•H2O | |
| D. | Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+═2Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23g钠与足量氧气充分反应,转移的电子个数为NA | |
| B. | 将1molFeCl3水解制成胶体,所得胶体的微粒数为NA | |
| C. | 1mol Na2O2与水完全反应时转移电子数为2NA | |
| D. | NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X | Y | Z |
| ① | N2 | Mg | CO2 |
| ② | KOH溶液 | SiO2 | 氢氟酸 |
| ③ | O2 | N2 | H2 |
| ④ | 稀硝酸 | Fe | FeCl3溶液 |
| A. | ①② | B. | ①③ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
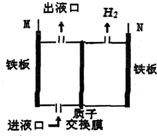 如图所示,某工厂采用电解法处理含铬(Cr2O72-)酸性废水,其中,耐酸电解槽以铁板作阴、阳极,电解后,溶液中的Cr2O72-全部变为Cr3+,下列说法不正确的是( )
如图所示,某工厂采用电解法处理含铬(Cr2O72-)酸性废水,其中,耐酸电解槽以铁板作阴、阳极,电解后,溶液中的Cr2O72-全部变为Cr3+,下列说法不正确的是( )| A. | M与电源的正极相连 | B. | 出液口排出的溶液中还含有Fe3+ | ||
| C. | N极电极反应为2H++2e-═H2↑ | D. | 阴极区附近溶液pH降低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com