
| A. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 在强碱溶液中:Na+、K+、SO32-、CO32- | |
| C. | 在c(H+)=10-13 mol•L-1的溶液中:NH4+、Al3+、SO42-、NO3- | |
| D. | 在pH=1的溶液中:K+、I-、Cl-、NO3- |
分析 A.铁离子与硫氰根离子反应生成络合物硫氰化铁;
B.四种离子之间不反应,都不与强碱性溶液中的氢氧根离子反应;
C.在c(H+)=10-13 mol•L-1的溶液为酸性或碱性溶液,铵根离子、铝离子与氢氧根离子反应;
D.pH=1的溶液中存在大量氢离子,硝酸根离子在酸性条件下能够氧化碘离子.
解答 解:A.Fe3+和SCN-之间反应生成硫氰化铁,在溶液中不能大量共存,故A错误;
B.强碱性溶液中存在大量氢氧根离子,Na+、K+、SO32-、CO32-之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.在c(H+)=10-13 mol•L-1的溶液中存在大量氢离子或氢氧根离子,NH4+、Al3+与氢氧根离子反应,在碱性溶液溶液中不能大量共存,故C错误;
D.pH=1的溶液为酸性溶液,I-、NO3-在酸性条件下发生氧化还原反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56g金属铁与一定量的硝酸反应时失去的电子数一定为3NA | |
| B. | 2mol SO2和1mol O2在密闭容器中加热(V2O5催化) 充分反应后,容器内分子总数为2NA | |
| C. | 1mol Cu和足量稀硝酸反应产生NA个NO分子 | |
| D. | 常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝基苯的结构简式: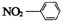 | B. | CO2分子比例模型: | ||
| C. | HClO的电子式: | D. | 中子数为10的氧原子:${\;}_{8}^{18}$O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向AlCl3溶液中加入过量浓氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 向澄清石灰水中通入少量CO2:OH-+CO2═HCO3- | |
| C. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| D. | NH4HCO3溶于过量的浓KOH溶液中:NH4++OH-═NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④>①>③>② | B. | ①>④>③>② | C. | ①=④>③=② | D. | ④=①>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、K+、CO32-、Cl- | B. | Ba2+、Na+、SO42-、NO3- | ||
| C. | Ca2+、Na+、NO3-、Cl- | D. | H+、Na+、OH-、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com