
| A. | 使酚酞变红色的溶液:NH4+、Al3+、NO3-、CO32- | |
| B. | 0.1 mol•L-1NaHCO3溶液:Na+、Ba2+、NO3-、OH- | |
| C. | 滴加KSCN溶液显红色的溶液:NH4+、K+、Cl-、NO3- | |
| D. | 由水电离出的c(H+)=10-12mol•L-1的溶液:Na+、K+、NO3-、ClO- |
分析 A.使酚酞变红色的溶液为碱性溶液,溶液中存在大量的氢氧根离子,铵根离子、铝离子与氢氧根离子反应,铝离子、碳酸根离子发生双水解反应;
B.碳酸氢钠与氢氧根离子反应生成碳酸钠和水,碳酸钠与钡离子反应生成碳酸钡沉淀;
C.滴加KSCN溶液显红色的溶液中存在大量的铁离子,四种离子之间不反应,都不与铁离子反应;
D.由水电离出的c(H+)=10-12mol•L-1的溶液中存在大量的氢离子或氢氧根离子,次氯酸根离子与氢离子反应生成次氯酸.
解答 解:A.使酚酞变红色的溶液中存在大量的氢氧根离子,NH4+、Al3+与氢氧根离子反应,Al3+、CO32-之间发生双水解反应,在溶液中不能大量共存,故A错误;
B.NaHCO3与Ba2+、OH-反应生成碳酸钡沉淀,在溶液中不能大量共存,故B错误;
C.滴加KSCN溶液显红色的溶液中含有铁离子,NH4+、K+、Cl-、NO3-之间不反应,都不与铁离子反应,在溶液中能够大量共存,故C正确;
D.由水电离出的c(H+)=10-12mol•L-1的溶液为酸性或碱性溶液,溶液中存在大量的氢离子或氢氧根离子,ClO-与氢离子结合生成次氯酸,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查了离子共存的判断,题目难度中等,注意熟练掌握离子性质及离子反应发生条件,明确题干暗含条件的含义及离子能够共存的条件,试题侧重考查学生的分析能力及逻辑推理能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | N=O | C≡O | C=O | N≡N |
| 键能(kj/mol) | 632 | 1072 | 750 | 946 |
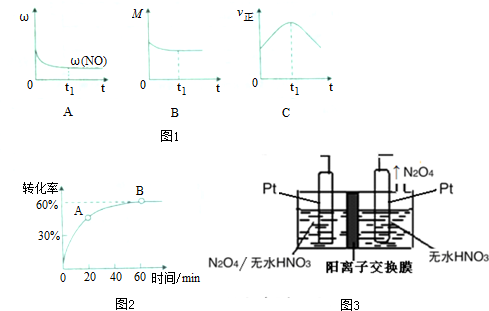
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④③①⑤ | B. | ②③⑤① | C. | ④⑥③① | D. | ③⑥⑤① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定含有的离子是③④⑤ | B. | 肯定没有的离子是②⑤ | ||
| C. | 可能含有的离子是①⑥ | D. | 不能确定的离子是③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | 开始沉淀pH | 完全沉淀pH |
| Fe3+ | 2.1 | 3.2 |
| Al3+ | 4.1 | 5.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com