
分析 根据CO2的体积,求出C的质量和物质的量,根据水的质量,求出H的质量和物质的量,根据质量守恒,确定有机物中是否含有氧,以此该求出有机物的分子式以及可能的结构简式.
解答 解:n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,n(H)=n(H2O)×2=0.6mol,m(H)=0.6g;
n(CO2)=$\frac{4.48L}{22.4L/mol}$=0.2mol,n(C)=n(CO2)=0.2mol,m(C)=2.4g,
m(C)+m(H)=3g,因有机物的质量为3g,所以有机物中没有氧元素,
因有机物的质量为4.6g,所以有机物中含有氧元素,氧元素的质量为1.6g,n(O)=$\frac{1.6g}{16g/mol}$=0.1mol,
则有机物的实验式为C2H6O,因碳原子已饱和,所以分子式为C2H6O,
可能为CH3CH2OH或CH3OCH3,
答:有机物最简式为C2H6O,分子式为C2H6O,可能的结构简式为CH3CH2OH或CH3OCH3.
点评 本题考查有机物分子式、结构式的确定等,难度中等,注意掌握官能团的性质,注意利用质量守恒确定氧元素,根据实验式中C、H数目关系确定分子式.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:解答题

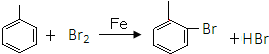 .
. .
.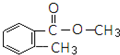 .
. 或
或  的邻、间、对的任意一种.
的邻、间、对的任意一种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在硫酸铜溶液中加入过量氢氧化钡溶液 Ba2++SO42-=BaSO4↓ | |
| B. | 钠与水的反应Na+2H2O═Na++2OH-+H2↑ | |
| C. | 氯气通入氢氧化钠溶液中 2Cl2+2OH-=3Cl-+ClO-+H2O | |
| D. | 大理石溶于醋酸的反应CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 研究金属铁及其化合物的性质有重要意义.
研究金属铁及其化合物的性质有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 用途 | 解释 |
| A | 硅胶可作袋装食品的干燥剂 | 硅胶多孔,吸收空气中氧气的能力强 |
| B | CuSO4可作游泳池的消毒剂 | 铜盐能使构成病毒的蛋白质变性 |
| C | 浸有高锰酸钾溶液的硅藻土可作某些水果的保鲜剂 | 高锰酸钾溶液能氧化水果释放的催熟剂乙烯 |
| D | Na2O2可作呼吸面具中的供氧剂 | Na2O2能吸收CO2同时放出O2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
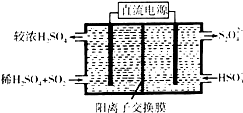 (1)利用Na2SO3溶液可脱除烟气中的SO2.Na2SO3可由NaOH溶液吸收SO2制得.NaOH溶液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如表:
(1)利用Na2SO3溶液可脱除烟气中的SO2.Na2SO3可由NaOH溶液吸收SO2制得.NaOH溶液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如表:| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{y-2x}{a}$ mol/L | B. | $\frac{y-x}{a}$ mol/L | C. | $\frac{2y-2x}{a}$ mol/L | D. | $\frac{2y-4x}{a}$mol/L |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高一上月考二化学试卷(解析版) 题型:选择题
下列现象或新技术应用中,不涉及胶体性质的是( )
A.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀
B.使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
C.江河入海口常形成三角洲
D.肾衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com