
【题目】短周期元素W、X、Y、Z的原子序数依次增大,这些元素组成的单质和化合物转化关系如下图所示。其中C是淡黄色固体,B和E的水溶液均具有漂白性。下列说法不正确的是

A. 阴离子半径;Y>Z>X
B. 沸点:D<A
C. 气态氢化物稳定性:Z>Y
D. 0.1mol·L-1A溶液中:e(H-)>c(HY-)>e(Y2-)
【答案】B
【解析】由图可知:C是淡黄色固体,是硫单质,B和E的水溶液均具有漂白性,B为SO2 ,E为 Cl2,A为H2S,D为H2O,F、G为硫酸和盐酸,短周期元素W、X、Y、Z的原子序数依次增大,这些元素分别是:W-H、X-O、Y-S、Z-Cl。
A、同周期自左而右阴离子半径减小,同主族从下而上阴离子半径减小,阴离子半径:Y>Z>X,故A正确;B、D为水,水分子间形成氢键,沸点高,沸点:D>A,故B错误;C、 气态氢化物稳定性HCl比H2S稳定,即Z>Y,故C正确;D.H2S是二元弱酸,分两步电离,第二步电离更弱 0.1mol·L-1H2S溶液中:e(H-)>c(HY-)>e(Y2-),故D正确;故选B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z原子序数依次增大,甲、乙、丙、丁均是由前3种元素组成的二元“10电子”微粒,能发生如图转化,Z的原子半径是所有短周期主族元素中最大的,下列说法错误的是

A. 原子半径大小:W<Y<X<Z
B. W、X、Y三种元素形成的化合物水溶液一定显酸性
C. W、X、Y与Z均能形成离子化合物
D. Y分别与其他三种元素至少可以形成两种化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。下列说法正确的是
A. 标准状况下,2.24L三氯甲烷中所含分子数为NA
B. 1molH2与1molI2(g)于密闭容器中反应,生成的H-I键数为2NA
C. 常温下,0.1molFe投入到足量浓硫酸中反应,转移的电子数为0.3NA
D. 8.8g乙酸乙酯和乙醛(CH3CHO)的混合物中含有的C原子数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸盐和金属硫化物在工农业生产中有广泛的应用。
(1)已知:
反应Ⅰ:CaSO4(s)+CO(g)=CaO(s)+SO2(g)+CO2(g)△H1=+218.4 kJ·mol-1
反应Ⅱ:CaSO4(s)+4CO(g)=CaS(s)+4CO2(g) △H2=-175.6kJ·mol-1
反应 Ⅲ:3CaSO4(s)+CaS(s)=4CaO(s)+4SO2(g) (B) △H3
①△H3=__________。
②能使反应Ⅰ、Ⅱ速率加快的措施有____________________________________(写出两条)。
③已知某温度下反应Ⅰ的反应速率小于反应Ⅱ的反应速率,则图1中曲线a表示__________ (填“反应Ⅰ”或“反应Ⅱ”)。


(2)在2L密闭容器中,加入0.1molMoS2(硫化钼)、0.2molNa2CO3和0.4molH2,发生反应MoS2(s)+2Na2CO3 (s)+4H2(g)![]() Mo(s)+2CO(g)+4H2O(g)+2Na2S(s),达到平衡时三种气体的物质的量分数随温度变化的曲 线如图2所示。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s),达到平衡时三种气体的物质的量分数随温度变化的曲 线如图2所示。
①反应速率:P点______ Q点(填“<” “>”或“=”),其判断理由是_____________。
②气体总压:P点__Q点(填“<” “>”或“=”),其判断理由是_____________。
③P点对应温度下,H2的平衡转化率为__________,平衡常数K=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种常用的植物调味油,工业上可按如下路线合成。

已知:
①有机物A是分子中单键与双键数目之比为4∶1的烯烃;
②G的分子式为C9H8O,能发生银镜反应;
③CH3CHO+CH3CHO![]()
![]() 。
。
回答下列问题:
(1)B的名称为__________,F中含有的官能团的名称是__________。
(2)E的结构简式为__________,G的结构简式为________________。
(3)⑤的反应类型为__________,⑥的反应类型为__________。
(4)反成③的化学方程式为_____________________________。
(5)反应①~⑥中符合原子经济性(原子利用率为100%)的是__________ (填序号)。
(6)同时符合下列条件的F的同分异构体有__________种,其中核磁共振氢谱显示有四组峰,且峰面积之比为3∶3∶2∶2的是__________ (填结构简式)。
a.苯环上含有两个取代基 b.分子中含有-COO-结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用铝锂钴废料(主要成分为Co3O4,还含有少量铝箔、LiCoO2等杂质)回收CoO的工艺流程如下:

回答下列问题:
(1)“碱溶”的目的是:________________。
(2)不同浸出剂“酸溶”实验结果见下表,根据数据和物质性质应选择的浸出剂是___________(填序号),理由是__________ (用Co3O4参与反应的离子方程式表示)。
浸出剂 | 浸出液化学成分/(g·L-1) | 钴浸出率/% | |
Co | Al | ||
(a)HCI | 80.84 | 5.68 | 98.4 |
(b)H2SO4 | 65.0 | 6.22 | 72.3 |
(c)H2SO4+ Na2S2O3 | 84.91 | 5.96 | 98.0 |
(3)“净化”产生的滤渣为____________(填化学式),滤液③中c(F-)=4.0×10-3mol·L-1,则“净化”后残余c(Li+)=___________。LiF与Li2CO3的Ksp分别为1.8×10-3、1.7×10-3。
(4)若滤液④中含Co2+为5.9×10-2g·L-1,“沉碳酸钴"应控制pH不高于___________。Co(OH)2的Ksp为1.0×10-15。
(5)“沉碳酸钴“→“沉草酸钻”的目的是___________。
(6)CaC2O4·H2O在空气氛围中的热重曲线如下图。在311.96℃附近有个很强的放热峰的原因是______。900℃发生反应的化学方程式为___________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,反应X2(g)+H2(g)![]() 2HX(g)的平衡常数为100。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于( )
2HX(g)的平衡常数为100。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于( )
A. 5% B. 17% C. 25% D. 33%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列 11 种物质:
①纯碱 ②Mn2O7 ③硫酸 ④CaO ⑤CO2 ⑥Na2CO3
⑦CuSO4·5H2O ⑧SO2 ⑨Na2O2 ⑩CO NO2
其中属于正盐的是______________;属于酸性氧化物的是__________________。
(2)有关胶体的实验中:
①实验室制备Fe(OH)3胶体的化学方程式为_________
②将橘红色的硫化锑(Sb2S3)胶体,装入U形管,插入电极后通直流电,发现阳极负极橘红色加深,证明Sb2S3胶粒带______(填“正”或“负”)电荷。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常认为残留在溶液中的离子浓度小于1×10-5mol/L时,离子不存在。图为H3PO4(图中用H3A表示)在加入强酸或强碱溶液后,平衡时溶液中各微粒浓度的对数值(lgc)-pH图。下列说法不正确的是( )
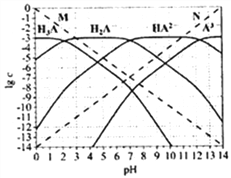
A. H3PO4、H2PO4-、HPO42-、PO43-不能在同一溶液中大量共存
B. H3PO4电离平衡常数Ka2≈1×10-7
C. 图中虚线M、N分别代表H+和OH-
D. pH=10时,溶液中存在关系:c(HPO42-)>c(OH-)>c(PO43-)>c(H2PO4-)>c(H3PO4)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com