
【题目】(1)写出铜原子价电子排布式:______。与铜同一周期的副族元素原子中最外层电子数与铜原子的相同的元素有________(填元素符号)。
(2)第三周期第一电离能处于Al和P之间的元素有______种。
(3)某种原子的结构示意图为![]() 。则该原子的核电荷数x取值范围为______。
。则该原子的核电荷数x取值范围为______。
(4)Cr在周期表中位于_____周期___族,属于___区,价电子排布图为______
(5)ClO4-互为等电子体的分子或离子为____。
(6)Ni与CO能形成配合物Ni(CO)4,该分子中π键与σ键个数比为_____。
【答案】3d104s1 Cr 3 20≤x≤30且X不等于24和29 四 VIB d 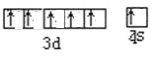 SO42-或其他合理答案 1:1
SO42-或其他合理答案 1:1
【解析】
(1)Cu原子3d、4s能级上电子为其价电子,3d能级上有10个电子、4s能级上有1个电子,其价电子排布式为3d104s1;
铜原子最外层排布为4s1,同周期外层排布为4s1,副族中d能级含有5个电子为Cr;
(2)同一周期元素,元素的第一电离能随着原子序数的增大而呈增大趋势,但同一周期中第ⅡA族元素比第ⅢA族元素的第一电离能大,第ⅤA族比第ⅥA族第一电离能大,Mg、Al、Si、P、S、Cl属于同一周期且其原子序数依次增大,但Mg属于第ⅡA元素,Al属于第ⅢA族,P属于第VA元素,S属于第ⅥA族,所Mg、Al、Si、P、S、Cl几种元素的第一电离能的大小顺序是P、S、Si、Mg、Al,所以第一电离能处于Al、P之间的元素有3种;
(3) 某种原子的结构示意图为![]() ,第三层电子数8≤y≤18,则该原子的核电荷数x取值范围为20≤x≤30,根据各能级的能量递增可知,x不等于24和29,故答案为20≤x≤30且x不等于24和29;
,第三层电子数8≤y≤18,则该原子的核电荷数x取值范围为20≤x≤30,根据各能级的能量递增可知,x不等于24和29,故答案为20≤x≤30且x不等于24和29;
(4)Cr为24号元素,在周期表中位于第四周期VIB族,属于d区,价电子排布图为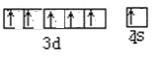 ;
;
(5)原子总数相同、价电子总数相同的微粒互为等电子体,与ClO4-互为等电子体的一种分子为CCl4,离子有SO42-;
(6)Ni与CO能形成配合物Ni(CO)4,CO中含有1个σ键,2个π键,配位键也属于共价键,也为σ键,该分子中σ键为: 1×4+4=8,π键个数为: 2×4=8,二者的比值为1:1。


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】298K时,将20mL3xmol·L-1Na3AsO3、20mL3xmol·L-1I2和20mLNaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-(aq)![]() AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43- 与反应时间(t)的关系如图所示。下列不能判断反应达到平衡的是
AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43- 与反应时间(t)的关系如图所示。下列不能判断反应达到平衡的是

A. 溶液的pH不再变化
B. 2v正(I-)=v逆(AsO33-)
C. c(AsO43-)/c(AsO33-)不再变化
D. c(I-)=2ymol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是降低润滑油凝固点的高分子有机化合物,其结构简式为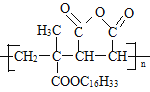 ,用石油裂解气合成M的路线图如图:
,用石油裂解气合成M的路线图如图:
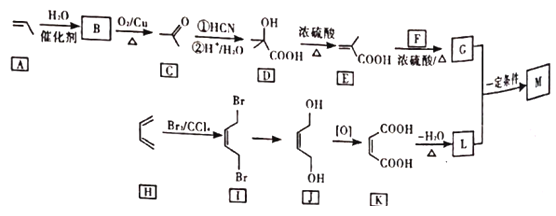
回答下列问题:
(1)B的化学名称为______。
(2)F的分子式为_____。
(3)G中官能团的名称是_____,G与L在一定条件下生成M的反应类型为____。
(4)I→J的反应方程式为_____。
(5)写出2种符合条件的C的同分异构体的结构简式____。(核磁共振氢谱为三组峰,峰面积比为3:2:1;已知双键和羟基相连时物质不稳定)
(6)设计由苯乙烯为起始原料制备![]() 的合成路线(无机试剂任选)____。
的合成路线(无机试剂任选)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
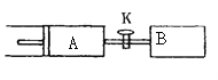
【题目】如图所示,向A、B中均充入1mol X、lmol Y,起始时A、B的体积都等于a L,在相同温度、外界压强和催化剂存在的条件下,关闭活塞K,使两容器中都发生下述反应: X(g)+Y(g)![]() 2Z(g)+W(g) △H<0。达平衡时,A的体积为1.4a L。下列说法错误的是( )
2Z(g)+W(g) △H<0。达平衡时,A的体积为1.4a L。下列说法错误的是( )
A.反应速率:![]()
B.平衡时的压强:![]()
![]()
C.A容器中X的转化率为80%
D.平衡时Y体积分数:A<B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置可验证同主族元素非金属性的变化规律
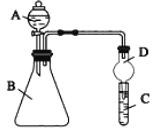
(1)仪器B的名称为________,干燥管D的作用为________。
(2)若要证明非金属性;![]() ,则A中加浓盐酸,B中加
,则A中加浓盐酸,B中加![]() ,(
,(![]() 与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,C溶液中的离子方程式为________,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用________溶液吸收尾气。
与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,C溶液中的离子方程式为________,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用________溶液吸收尾气。
(3)若要证明非金属性:![]() ,则在A中加盐酸,B中加
,则在A中加盐酸,B中加![]() ,C中加________(写化学式)溶液,若观察到C中出现白色沉淀,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有________溶液的洗气瓶。
,C中加________(写化学式)溶液,若观察到C中出现白色沉淀,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有________溶液的洗气瓶。
查看答案和解析>>
科目:高中化学 来源: 题型:
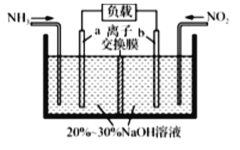
【题目】利用反应NO2+NH3→N2+H2O(未配平)消除NO2的简易装置如图所示。下列说法不正确的是( )
A.a电极反应式是![]()
B.消耗标准状况下![]() 时,被消除的NO2的物质的量为
时,被消除的NO2的物质的量为![]()
C.若离子交换膜是阳离子交换摸,装置右室中溶液的碱性增强
D.整个装置中NaOH的物质的量不断减少
查看答案和解析>>
科目:高中化学 来源: 题型:
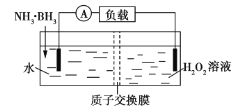
【题目】氨硼烷(NH3·BH3)电池可在常温下工作,装置如图所示。未加入氨硼烷之前,两极室质量相等,电池反应为NH3·BH3+3H2O2==NH4BO2+4H2O 。已知H2O2足量,下列说法正确的是( )
A. 正极的电极反应式为2H++2e-===H2↑
B. 电池工作时,H+通过质子交换膜向负极移动
C. 电池工作时,正、负极分别放出H2和NH3
D. 工作足够长时间后,若左右两极室质量差为1.9 g,则电路中转移0.6 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中充入0.3molA、0.1molC和一定量的B三种气体。一定条件下发生反应,各物质的浓度随时间变化如甲图所示[t0~t1阶段的c(B)变化未画出]。乙图为t2时刻后改变条件时平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同,t3~t4阶段为使用催化剂。下列说法中不正确的是
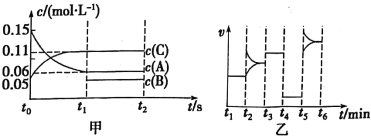
A.若t1=15s,则用A的浓度变化表示的t0~t1阶段的平均反应速率为0.006mol·L-1·s-1
B.t4~t5阶段改变的条件一定为减小压强
C.该容器的容积为2L,B的起始物质的量为0.02mol
D.该反应的化学方程式为3A![]() B+2C
B+2C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是
A.“神舟六号”飞船返回舱的表层采用高温时自动烧蚀的耐高温、抗氧化的新型无机非金属材料带走热量从而保证内部温度不致过高。
B.“加碘食盐”“含氟牙膏”“富硒营养品”“高钙牛奶”“加铁酱油”等等,这里的碘、氟、硒指的是分子,钙、铁则分别是钙离子和铁离子。
C.下图是反应物和生成物的能量变化示意图,则其可能发生的反应的热化学方程式可表示为:2A(g)+B(g)=2C(g);△H=QkJ/mol(Q>0)
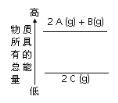
D.已知4P(红磷,s)=P4(白磷,s);△H>0,则白磷比红磷稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com