
| A�� | Ҫ�ӳȺ�ɫҺ���з���������壬�ɲ�ȡ�IJ��������� | |
| B�� | ������Ϊ���ˣ���ҪĿ����Ϊ�˳�ȥ MgSO4 | |
| C�� | �Լ� CΪK2CO3������D��ҪΪMg��OH��2��BaSO4������������BaCO3 | |
| D�� | ���ڲ����ܽ���������Һ���л��ǣ�Ӧ��ȡ�Ĵ�ʩ�Ǹ�����ֽ�����¹��� |
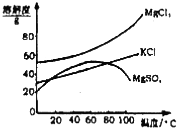
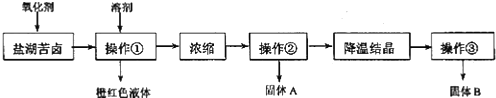
���� ��ͼ1���̲���Ϊ���κ���±��Ũ��Һ�м���������ӦΪ�������������壬ͨ����ȡ����Һ�ķ������룬Ũ����õ�����þ���Ȼ��صĻ��Һ�����ؽᾧ�ɵ�����þ�����˵õ��Ȼ�����Һ�������½ᾧ�����˿ɵõ��Ȼ��أ�
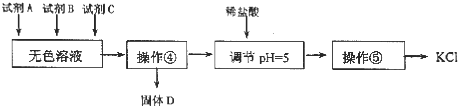
�����������ٺ���ɫ��Һ����K+��Mg2+��SO42-��Cl-�����ӣ���ɫ��Һ���ȼ��Լ�A��KOH�����Գ�ȥMg2+���ټ��Լ�B��BaCl2���Գ�ȥSO42-�������Լ�K2CO3���ɳ�ȥ�����ı����ӣ����˿ɵõ�Mg��OH��2��BaSO4�����Լ�����BaCO3������Ȼ���������ɳ�ȥ�������������غ�̼��أ���������Ũ������ȴ�ᾧ�ɵõ��Ȼ��أ�
A��������ܽ��Һ�����÷е�IJ�ͬ����������ķ����ķ��룻
B�������ڱ�����ȹ��ˣ�
C�����ݲ����ٺ���ɫ��Һ����K+��Mg2+��SO42-��Cl-�Լ�ʵ���Ŀ������ȡ�ϴ������Ȼ��ؾ��壬�������������س�ȥMg2+�������Ȼ�����ȥSO42-���������̼��س�ȥ�������Ȼ�����
D����Һ���л��ǣ�˵����ֽ������Ҫ������ֽ�����¹��ˣ�
��� �⣺A�������л��ܼ����ܣ����е�IJ�ͬ����������ķ����ķ��룬��A��ȷ��
B������þ�ڸ������ܽ�Ƚ�С���Ȼ����ڸ���ʱ�ܽ�ȴ��ó��ȹ��ˣ��ܳ�ȥ��������������þ����ֹ�Ȼ�����ȴ�����������Բ�����Ϊ���ȹ��ˣ���B����
C�������ٺ���ɫ��Һ����K+��Mg2+��SO42-��Cl-�Լ�ʵ���Ŀ������ȡ�ϴ������Ȼ��ؾ��壬�������������س�ȥMg2+�������Ȼ�����ȥSO42-���������̼��س�ȥ�������Ȼ������õ��ij���Ϊ������þ�����ᱵ��̼�ᱵ����C��ȷ��
D����Һ���л��ǣ�˵����ֽ��������Ӧ������ֽ�����¹��ˣ���D��ȷ��
��ѡB��
���� ���⿼�������ʷ������ᴿ�������ۺ�Ӧ�ã���Ŀ�Ѷ��еȣ���ȷʵ��Ŀ�ġ�ʵ��ԭ��Ϊ���ؼ���ע�������������ʷ������ᴿ�ij��÷�������������������ķ�����������ѧʵ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȡ����Ӧ | B�� | �ӳɷ�Ӧ | C�� | ������Ӧ | D�� | ������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ֻ��Na2CO3 | |
| B�� | ԭ���������O2��CH4�����ʵ���֮��Ϊ1�s2 | |
| C�� | ������ֻ��NaOH | |
| D�� | ԭ���������O2��CH4�������Ϊ2�s1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶�Ĵ�С˳��Ϊ��rX��rY��rZ��rW��rQ | |
| B�� | Z��Q�γɵĻ�����Ϊ���ӻ����� | |
| C�� | ��������Ԫ��Z��Ԫ��W�γɵĻ������ˮ��Һ | |
| D�� | Ԫ��W������������Ӧ��ˮ��������Ա�Q��ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
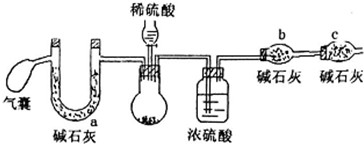
| ��������Ũ�ȣ�mol•L-1�� | 5 | 2 | 1 | 0.01 |
| ��Һ������ɫ��ʱ�䣨s�� | 8 | 94 | 450 | ��ʱ�䲻��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
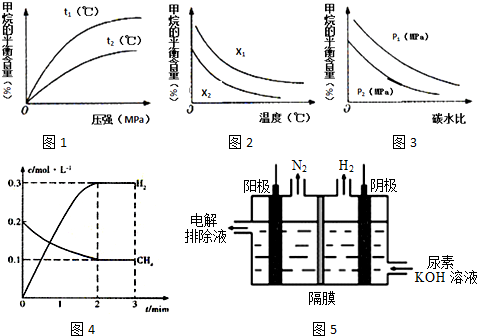
| t/min | n��CH4��/mol | n��H2O��/mol | n��CO��/mol | n��H2��/mol |
| t1 | 0.18 | 0.38 | 0.22 | 0.66 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 SO2���������γ����꣬Σ�������������Ƽ�ѭ�������ѳ������е�SO2��
SO2���������γ����꣬Σ�������������Ƽ�ѭ�������ѳ������е�SO2��| n��SO32-������n��HSO3-�� | 91��9 | 1��1 | 1��91 |
| PH | 8.2 | 7.2 | 6.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com