
【题目】完成下列化学用语:
(1)画出 O2﹣结构示意图:_____,某种核素质量数 37,中子数 20,其原子符号:_____
(2)写出实验室制氯气的化学方程式:______________________
(3)工厂里常用浓氨水来检验氯气管道是否泄漏,其原理为:8NH3+3Cl2=6NH4Cl+N2,请用双线桥表示其电子转移的方向和数目__________________________________
【答案】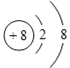
![]() MnO2+4HCl(浓)
MnO2+4HCl(浓) ![]() MnCl2+C12↑+2H2O
MnCl2+C12↑+2H2O 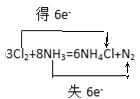
【解析】
(1)O2﹣核外有10个电子;某种核素质量数为 37、中子数为 20,质子数是17,属于氯元素。
(2)实验室用二氧化锰和浓盐酸加热制取氯气;
(3)8NH3+3Cl2=6NH4Cl+N2反应中氯元素化合价由0降低为-1,氮元素化合价由-3升高为0。
(1)O2﹣核外有10个电子,结构示意图是 ;某种核素质量数为 37、中子数为 20,质子数是17,属于氯元素,原子符号是
;某种核素质量数为 37、中子数为 20,质子数是17,属于氯元素,原子符号是![]() 。
。
(2)二氧化锰和浓盐酸加热生成氯化锰、氯气、水,反应方程式是MnO2+4HCl(浓) ![]() MnCl2+C12↑+2H2O;
MnCl2+C12↑+2H2O;
(3)8NH3+3Cl2=6NH4Cl+N2反应中氯元素化合价由0降低为-1,氮元素化合价由-3升高为0,电子转移的方向和数目是 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某干燥粉末可能由Na2O、Na2O2、Na2CO3、NaHCO3、NaCl中的一种或几种组成。将该粉末与足量的盐酸反应有气体X逸出,X通过足量的NaOH溶液后体积缩小(同温、同压下测定),且有气体剩余。若将原来混合粉末在空气中用酒精灯加热,也有气体放出,且剩余固体的质量大于原混合粉末的质量。下列判断正确的是
①粉末中一定有Na2O、Na2O2、和NaHCO3
②粉末中一定不含有Na2CO3和NaCl
③粉末中一定不含有Na2O2和NaCl
④无法肯定粉末中是否含有Na2CO3和NaCl
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是某学生设计的实验室制备并干燥Cl2及吸收多余氯气的实验装置图,请回答:

(1)指出上图中的各处错误:
①____________________________________________________
②____________________________________________________
③____________________________________________________
④____________________________________________________
(2)制备实验开始时,先检查装置的气密性,接下来的操作依次是 ________
A、向烧瓶中加入MnO2粉末 B、加热 C、向烧瓶中加入浓盐酸
(3)如果将过量二氧化锰与20mL 12mol·L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06mol。其主要原因有:
①____________________________________________________
②____________________________________________________
(4)为了提高浓盐酸的利用率,你对实验的建议是:
①____________________________________________________
②____________________________________________________
(5)写出圆底烧瓶中发生反应的离子反应方程式,并用单线桥表示电子转移的方向和数目________________
(6)NaClO是84消毒液的有效成分。请回答下列问题
①浸泡衣物时加入84消毒液在空气中放置一段时间漂白效果更好,结合离子方程式解释原因 ____________(已知酸性:H2CO3 >HClO>HCO3-)
②若将84消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是____________________________________________;
(7)Cl2是一种有毒气体,如果泄露会造成严重的危害。
①已知:3Cl2 + 8NH3 = 6NH4Cl +N2,化工厂可用浓氨水来检验Cl2是否泄露,该反应中被氧化和未被氧化的NH3的物质的量比________ ;
②喷射石灰乳等碱性物质可以减轻少量Cl2泄露造成的危害,Cl2与石灰乳反应的化学方程式是____________
③实验室常用烧碱溶液吸收Cl2,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合溶液。当NaCl和NaClO3的物质的量之比为15:2时,混合液中NaClO和NaClO3的物质的量之比为________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设 NA 表示阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,22.4L CCl4 含有的原子数为 5NA
B.1.8g 的 NH4+中含有的电子数为 NA
C.常温常压下,32 g O2 和 O3 的混合气体中所含原子数为 1.5 NA
D.7.1g Cl2 溶于水,转移电子数目为 0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香烃X(相对分子质量为92)是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A为一氯代物,H是通过缩聚反应获得的高聚物。

已知:![]() (苯胺,易被氧化)
(苯胺,易被氧化)
(1)X的结构简式为 。
(2)A的结构简式为 。
(3) G的结构简式为 。反应②③两步能否互换 ,(填“能”或“不能”)理由是 。
(4)反应④的化学方程式是 ;反应⑤的化学方程式是 。
(5)写出同时满足下列条件的阿司匹林的一种同分异构体的结构简式 。
①苯环上一卤代物只有2种;
②能发生银镜反应,分子中无甲基;
③1mol该物质最多能与3molNaOH反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 烯中C=C的键能是乙烷中C-C的键能的2倍
B. 氮气分子中含有1个s键和2个p键
C. N-O键的极性比C-O键的极性大
D. NH4+中4个N-H键的键能不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体的说法一定正确的是( )
A. 第ⅠA族碱金属元素与ⅦA族元素所形成的化合物在固态时为离子晶体,晶体中阴、阳离子排列方式相同
B. 晶体中存在阴离子就必定存在阳离子,存在阳离子就必定存在阴离子
C. 离子晶体中只含有离子键,分子晶体、原子晶体中必定含有共价键
D. C60晶体(其结构模型如图)中每个C60分子周围与它距离最近且等距离的C60分子有12个

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 新制的氯水在光照条件下颜色变浅
B. 合成氨工业中使用铁触媒作催化剂
C. 红棕色的NO2气体,加压后颜色先变深后变浅
D. 工业生产硫酸的过程中,通入过量的空气以提高二氧化硫的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,向20mL 0.1mol/L的醋酸溶液中不断滴加0.1mol/L的NaOH溶液,溶液的pH变化曲线如图所示,在滴定过程中,下列关于溶液中离子浓度大小关系的描述不正确的是
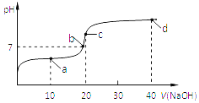
A. a点时:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-)
B. b点时:c(Na+) = c(CH3COO-)
C. c点时:c(OH-) =c(CH3COOH) + c(H+)
D. d点时:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com