
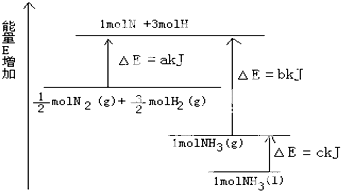
 已知化学反应N2+3H2═2NH3的能量变化如图所示:
已知化学反应N2+3H2═2NH3的能量变化如图所示:| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、可加入硫酸以提高电解质的导电性 |
| B、放电时电池内部Li+向负极移动. |
| C、充电过程中,电池正极材料的质量不变 |
| D、放电时电池正极反应为:FePO4+Li++e-=LiFePO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
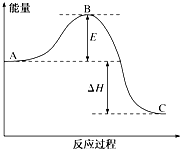 3H2(g)+N2(g)?2NH3(g) 反应过程中的能量变化如图所示.有关说法错误的是( )
3H2(g)+N2(g)?2NH3(g) 反应过程中的能量变化如图所示.有关说法错误的是( )| A、图中C表示生成物NH3(g)的总能量 |
| B、断裂3molH-H和1mol N≡N所吸收的总能量大于形成6mol N-H所释放的总能量 |
| C、逆反应的活化能E(逆)=E+△H |
| D、3 H2(g)+N2(g)?2NH3(g)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同周期元素随核电荷数的增加,第一电离能依次增大 |
| B、元素原子的最外层电子数等于元素的最高化合价 |
| C、同主族元素从上到下,单质的熔点逐渐降低 |
| D、第ⅦA元素从上到下,其氢化物的还原性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向Ba(OH)2溶液中加入过量的NH4HSO4溶液Ba2++2OH-+NH4++H++SO42-═BaSO4↓+NH3?H2O+H2O |
| B、工业上用石灰乳制漂粉精:2OH-+Cl2=Ca2++Cl-+ClO-+H2O |
| C、向漂白粉溶液中通入一定量的SO2Ca2++3ClO-+SO2+H2O=CaSO4+Cl-+2HClO |
| D、向100mL 0.1mol/L NaOH溶液中滴入数滴0.2mol/L Ca(HCO3)2溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com