
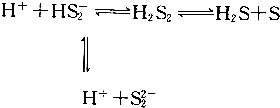
| A. | 该溶液中存在H2S分子 | |
| B. | 该溶液中H+的浓度是S${\;}_{2}^{2-}$浓度的2倍 | |
| C. | 向该溶液中加入足量的硝酸能产生H2S气体 | |
| D. | 向该溶液中加入过量的NaOH溶液可得到含大量NaHS2的混合溶液 |
分析 A.因为该反应是可逆反应,所以达到平衡后反应物和生成物共同存在于体系中;
B.因溶液中H+的来源有3个方面;
C.H2S是一种还原性气体,若加入的酸是氧化性酸,H2S将被氧化成硫;
D.NaHS2是一种酸式盐可以与NaOH反应.
解答 解:A.因为该反应是可逆反应,所以达到平衡后反应物和生成物共同存在于体系中,即存在H2S分子,故A正确;
B.因溶液中H+的来源有3个方面,即水的电离、HS2-和H2S2的电离,因此溶液中H+浓度不一定是S22-浓度的2倍,故B错误;
C.H2S是一种还原性气体,若加入的酸是氧化性酸,H2S将被氧化成硫,而不会放出H2S气体,故C错误;
D.NaHS2是一种酸式盐可以与NaOH反应,向该溶液中加入过量的NaOH溶液,生成Na2S2,不存在大量的NaHS2,故D错误;
故选:A.
点评 本题考查化学平衡状态的特点和外界条件对化学平衡的影响,明确反应的可逆性、不完全转化性、物质之间的化学反应是解答本题的关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 硫酸钡难溶于水,但硫酸钡属于强电解质 | |
| B. | 强电解质都是可溶性化合物,弱电解质都是难溶性化合物 | |
| C. | 氯化氢水溶液能导电,所以氯化氢是电解质 | |
| D. | 强电解质能够电离,弱电解质不能电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | OH-的电子式: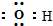 | |
| B. | F-的结构示意图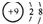 | |
| C. | N2的结构式: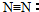 | |
| D. | 碳酸氢钠的电离方程式:NaHCO3=Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3- 在水溶液中只电离,不水解 | B. | 硝酸钠溶液水解后呈中性 | ||
| C. | 可溶性的铝盐都能发生水解反应 | D. | 可溶性的钠盐都不发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 反应① | 反应② |
| A | 向AgNO3溶液中滴加稀盐酸 | AgNO3溶液与食盐水混合 |
| B | 过量CO2通入NaOH溶液中 | 过量CO2通入澄清石灰水中 |
| C | 向烧碱溶液中滴加稀盐酸 | 向H2SO4溶液中滴加KOH溶液 |
| D | 向BaCl2溶液中滴加稀硫酸 | 向Ba(OH)2溶液中滴加CuSO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳碳双键
碳碳双键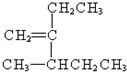 3-甲基-2-乙基-1-戊烯④
3-甲基-2-乙基-1-戊烯④ 2-甲基戊烷
2-甲基戊烷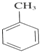 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$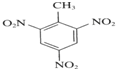 +3H2O.
+3H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1说明2molH2(g)和1molO2(g)的能量总和小于2molH2O(g)的能量 | |
| B. | 已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定 | |
| C. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4kJ•mol-1,则含20gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量 | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1; 2C(s)+O2(g)=2CO(g)△H2;则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子数相同的气体,它们的体积一定相等 | |
| B. | 高温时,气体体积一定比低温时的体积大 | |
| C. | 相同状况下,物质的量相同的两种气体的体积相同 | |
| D. | 压强大时,气体体积一定比压强小时的体积小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com