
分析 短周期元素A、B、C、D、E、F六种主族元素,原子序数依次增大,B原子的最外层电子数是次外层电子数的2倍,则B为C元素;D是地壳中含量最高的元素,则D为O元素;C的原子序数大于C小于O,则C为N元素;A元素的核外电子数等于电子层数,则A为H元素;E元素原子最外层只有1个电子,则E为Na元素;F与D元素处在同一主族,则F为S元素,据此结合元素周期律知识进行解答.
解答 解:短周期元素A、B、C、D、E、F六种主族元素,原子序数依次增大,B原子的最外层电子数是次外层电子数的2倍,则B为C元素;D是地壳中含量最高的元素,则D为O元素;C的原子序数大于C小于O,则C为N元素;A元素的核外电子数等于电子层数,则A为H元素;E元素原子最外层只有1个电子,则E为Na元素;F与D元素处在同一主族,则F为S元素,
(1)根据分析可知,A为H元素、B为C元素、D为O元素、E为Na元素,故答案为:H; C;O;Na;
(2)C为N元素,原子序数为7,位于周期表中第二周期VA族,故答案为:二;VA;
(3)A为H元素,H分别与B、C、D元素形成简单氢化物的化学式依次为:CH4、NH3、H2O,元素的非金属性越强,其气态氢化物的稳定性越强,则稳定性最强的为水,
故答案为:CH4、NH3、H2O;H2O;
(4)A、C、D形成的化合物为硝酸铵或硝酸,若为硝酸铵,则属于离子化合物,其化学式中含有离子键和共价键;若为硝酸,则属于共价化合物,含有共价键,
故答案为:离子(或共价);离子键和共价(或共价).
点评 本题考查了位置、结构与性质的关系,题目难度中等,正确推断各元素名称为解答关键,注意掌握元素周期表结构、元素周期律的内容,试题侧重考查学生的分析、理解能力.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:选择题
| A. | IA和VIIA族元素间可形成共价化合物 | |
| B. | 第二周期:从左到右最高价从+1到+7 | |
| C. | 同主族的单核阴离子:还原性越强,离子半径越小 | |
| D. | 同周期金属:原子失电子能力越强,最高化合价越高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水溶液能导电 | B. | 易溶于水 | C. | 熔化时能导电 | D. | 有较高的熔点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
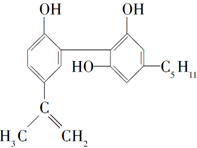 我国在反兴奋剂问题上的坚决立场是支持“人文奥运”的重要体现.某种兴奋剂的结构如下.关于它的说法正确的是( )
我国在反兴奋剂问题上的坚决立场是支持“人文奥运”的重要体现.某种兴奋剂的结构如下.关于它的说法正确的是( )| A. | 它的化学式为C19H26O3 | |
| B. | 该化合物只能发生取代反应 | |
| C. | 从结构上看,它属于醇类 | |
| D. | 从元素组成上看,它可以在氧气中燃烧生成CO2和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | C | |
| B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
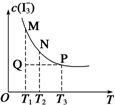 将I2溶于KI溶液中,能配制成浓度较大的碘水,主要是发生了反应:I2(aq)+I-(aq)?I3-(aq).该平衡体系中,I3-的物质的量浓度与温度(T)的关系如图所示(曲 线上的任何一点都代表平衡状态).下列说法正确的是( )
将I2溶于KI溶液中,能配制成浓度较大的碘水,主要是发生了反应:I2(aq)+I-(aq)?I3-(aq).该平衡体系中,I3-的物质的量浓度与温度(T)的关系如图所示(曲 线上的任何一点都代表平衡状态).下列说法正确的是( )| A. | 反应速率:vM>vP | B. | 平衡常数:KN<KP | ||
| C. | M、N两点相比,M点的c(I-)大 | D. | Q点时,v正>v逆 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com