
溴是海水中重要的非金属元素,地球上90%的溴元素以Br-的形式存在于海水中,所以人们称溴为“海洋元素”。下列有关说法中正确的是( )
A.从海水中提取溴时,不涉及氧化还原反应
B.苯与溴反应生成溴苯
C.可以用CCl4萃取溴水中的溴
D.向FeBr2溶液中通入Cl2时,一定会发生如下反应:
2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-
科目:高中化学 来源: 题型:
聚丙烯酸酯类涂料是目前市 场上流行的墙面涂料之一,其结构简式为:
场上流行的墙面涂料之一,其结构简式为: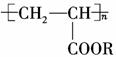 ,它具有弹性好、不易老化、耐擦洗、色泽亮丽等优点。下列对聚丙烯酸酯的叙述正确的是( )
,它具有弹性好、不易老化、耐擦洗、色泽亮丽等优点。下列对聚丙烯酸酯的叙述正确的是( )
①是缩聚产物 ②是加聚产物 ③属于混合物 ④属于纯净物 ⑤可以发生水解反应
A.①③⑤ B.②③⑤
C.①④⑤ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知:H2(g)+O2(g) H2O(g),反应过程中能量变化如图所示,则:
H2O(g),反应过程中能量变化如图所示,则:

①试写出a、b、c分别代表的意义:
a ;
b ;
c 。
②该反应是 反应(填“吸热”或“放热”),ΔH 0(填“>”或“<”)。
(2)发射“天宫”一号的火箭使用的推进剂是液氢和液氧,这种推进剂的优点是 , 。(请写两条)
(3)已知:H2(g)+O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
H2(g)==H2(l) ΔH=-0.92 kJ·mol-1
O2(g)==O2(l) ΔH=-6.84 kJ·mol-1
H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
请写出液氢和液氧生成气态水的热化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在4 L密闭容器中充入6 mol A气体和5 mol B气体,在一定条件下发生反应:3A(g)+B(g)2C(g)+xD(g),5 s达到平衡。达到平衡时,生成了2 mol C,经测定D的浓度为0.5 mol·L-1,下列判断正确的是
A.x=1
B.B的转化率为20%
C.平衡时A的浓度为1.50 mol·L-1
D.B的平均反应速率为0.2 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO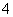 +H2C2O4+H+——Mn2++CO2↑+H2O(未配平)。用4 mL 0.001 mol·L-1KMnO4溶液与2 mL 0.01 mol·L-1H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
+H2C2O4+H+——Mn2++CO2↑+H2O(未配平)。用4 mL 0.001 mol·L-1KMnO4溶液与2 mL 0.01 mol·L-1H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2 | 20 | |
| Ⅱ | 2 | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2 | 30 | |
| Ⅳ | 1 | 20 | 1 mL蒸馏水 |
(1)该反应中氧化剂和还原剂的物质的量之比为________________________________________________________________________。
(2)如果研究催化剂对化学反应速率的影响,使用实验______和______(用Ⅰ~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,使用实验______和______。
(3)对比实 验Ⅰ和Ⅳ,
验Ⅰ和Ⅳ, 可以研究________对化学反应速率的影响,实验Ⅳ中加入1 mL蒸馏水的目的是__________________________________________
可以研究________对化学反应速率的影响,实验Ⅳ中加入1 mL蒸馏水的目的是__________________________________________ ________________________。
________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应广泛应用于金属冶炼,下列说法不正确的是( )
A.电解熔融氯化钠制取金属钠的反应中,钠离子被还原
B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应
C.用磁铁矿炼铁的反应中,1 mol Fe3O4被CO还原成Fe,转移9 mol 电子
D.铝热法还原铁的反应中,放出的热量能使铁熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中镁的总储量约为2.1×1015 t,目前世界上60%的镁来自海水。工业上从海水中提取镁的步骤为:
①将海水中大量存在的贝壳煅烧成石灰;②将石灰制成石灰乳;③将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)2沉淀;④在Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到Mg Cl2·6H2O;⑤将MgCl2·6H2O在一定条件下加热得到无水MgCl2;⑥电解熔融的MgCl2可得到镁。
Cl2·6H2O;⑤将MgCl2·6H2O在一定条件下加热得到无水MgCl2;⑥电解熔融的MgCl2可得到镁。
试回答下列问题:
(1)请写出海水提取镁的过程中①、⑥反应的化学方程式:
①____________________;⑥____________________。
(2)工业上采用电解MgCl2的方法制得金属镁,电解槽中阴极的电极反应式为:________________________________________________________________________。
(3)步骤⑤中的“一定条件”指的是_______,目的是_____________________。
(4)上述提取镁的流程中,可以在降低成本,减少污染方面做出一些工作,请写出其中一点______________________________________。
(5)有同学认为上述过程中,可加热Mg(OH)2得到MgO,再电解熔融MgO制金属镁,这样可简化实验步骤,体现实验的简约性原则。你同意该同学 的想法吗?为什么?_____________________________
的想法吗?为什么?_____________________________ ___________________________________________
___________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是
A.NaHCO3溶液与盐酸:CO32− + 2 H+ = H2O + CO2↑ B.硝酸银溶液与铜:Cu + Ag+ = Cu2+ + Ag
C.向硝酸亚铁溶液中加入稀硫酸:Fe2++4H++NO3-=Fe3++NO↑+2H2O
D.用醋酸除水垢:2CH3COOH + CaCO3 = Ca2+ + 2CH3COO− + H2O + CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D为四种短周期元素,已知A、C同主族,B、C、D同周期;A的气态氢化物比C的气态氢化物稳定;B的阳离子比D的阳离子氧化性强;B的阳离子比C的阴离子少一个电子层。下列叙述正确的是( )
A.原子序数:A>C>B>D B.单质熔点:D>B, A>C
C.原子半径:D>B>C>A D.简单离子半径:D>B>C>A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com