
�¶�ΪTʱ����2.0 L�����ܱ������г���2.0 mol NO2����Ӧ2NO2(g) N2O4(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
N2O4(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
t/s | 0 | 50 | 150 | 250 | 350 |
n(N2O4)/mol | 0 | 0.12 | 0.18 | 0.20 | 0.20 |
����˵����ȷ����
A����Ӧ��ǰ50 s��ƽ������Ϊv(NO2)��0.001 2 mol��L��1��s��1
B�������¶Ȳ��䣬��ƽ���������г���1.0 mol N2O4ʱ��v(��)<v(��)
C�����������������䣬�����¶ȴﵽ��ƽ��ʱK��0.125����Ӧ�Ħ�H<0
D��T�¶�ʱ������ʼ�������г���2.0 mol N2O4����ƽ��ʱN2O4��ת���ʴ���80%
BC
��������
���������A����Ӧ��ǰ50 s��ƽ������v��NO2����2v��N2O4��=0.002 4 mol��L��1��s��1������B�������¶Ȳ��䣬��ƽ���������г���1.0 mol N2O4ʱ��ƽ�����ƣ�v(��)<v(��)����ȷ��C���¶�ΪTʱ��K��T����0.156��0.125��K�������¶ȣ�ƽ�����ƣ�������ӦΪ���ȷ�Ӧ����ȷ��D������4.0 L�����г���2.0 mol N2O4���ﵽƽ��ʱ��N2O4��ת����Ϊ80%��������ѹ��Ϊ2.0 Lʱ��ƽ��������N2O4�ķ����ƶ�����N2O4��ת����С��80%������
���㣺���黯ѧ��Ӧ���ʡ���ѧƽ�⡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡտ���б�ҵ����в������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ���������ֵ������˵����ȷ����
A��1mol�����Ӻ���3NA��C��C��
B��һ�������£�1mol N2��3mol H2��ֻ�ϣ���Ӧ��ת�Ƶĵ�����Ϊ6NA
C�������£�78.0g Na2O2��58.5g NaCl���������������
D����״���£�2.24L CCl4����������Ϊ0.1 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�γ��С��������и�һ��ѧ������������ѧ�Ծ��������棩 ���ͣ������
(10��)��Ȼ���е����ʶ������Ի�������ʽ���ڣ������ǻ����ķ�����ᴿҪ������գ�
��1����ȥNaCl�е�Na2SO4�����μ������ҺΪ�������ʻ�ѧʽ����______��______��________��
��2����ͼ�dz��õ�ʵ������������̨�Ͳ������ܡ���Ƥ�ܡ�ƿ������ȥ��
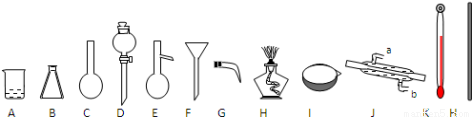
����д�������������ƣ�D ��J ��
�������Ȼ�̼��ȡ��ˮ��Br2���ʣ���ȡ�ܷ��þƾ��������Ȼ�̼����ʵ�飿 ��������ԭ�� ��
������װ���У���E�м����ʯ��Ŀ���� ������J������ˮӦ�� �� ������дa��b����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�γ��С��������и�һ��ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
����������NH4Cl��NaCl��Na2CO3�������ʵ��Լ�(��Ҫʱ���Լ���)��
A��AgNO3��Һ B��ϡ���� C��ϡ���� D��Ba(OH)2��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и�����ѧ�ڵ�һ�ν��Բ��Ի�ѧ�Ծ��������棩 ���ͣ������
����þ����������Ͻ𡢴�����ϡ�þ��صȡ�
��֪:��C(s)+O2(g) CO(g) ��H=-110.5 kJ��mol-1��Mg(g)+O2(g)
CO(g) ��H=-110.5 kJ��mol-1��Mg(g)+O2(g) MgO(s) ��H=-732.7 kJ��mol-1
MgO(s) ��H=-732.7 kJ��mol-1
��1��һ���Ʊ�þ�ķ�ӦΪMgO(s)+C(s) Mg(g)+CO(g),�÷�Ӧ�Ħ�H= ��
Mg(g)+CO(g),�÷�Ӧ�Ħ�H= ��
��2��һ����ˮ��þʯ(��Ҫ�ɷ�ΪMgCl2��6H2O)�ƽ���þ���յĹؼ���������:
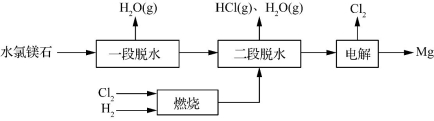
��Ϊ̽��MgCl2��6H2O��һ����ˮ���ĺ����¶ȷ�Χ,ij����С�齫MgCl2��6H2O�ڲ�ͬ�¶��·ֽ�,��ò����������ʵ�X-����������ͼ����ͼ��ʾ(X-��������������ж�ij��̬�����Ƿ����)�����E��MgԪ����������Ϊ60.0%,��E�Ļ�ѧʽΪ �� ��һ����ˮ����Ŀ�����Ʊ�MgCl2��2H2O,�¶Ȳ�����180 ���ԭ���� ��
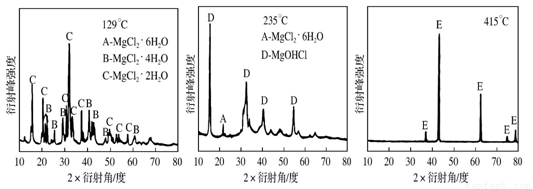
�������ʱ��������ˮ��,�����ɵ�MgOHCl������������Mg��Ӧ,ʹ�����������MgO�ۻ�Ĥ,���͵��Ч�ʡ�����MgO�Ļ�ѧ����ʽΪ ��
��3��Mg2Ni��һ�ִ�����ϡ�2.14 g Mg2Ni��һ��������������0.896 L H2(��״����)����X��X�Ļ�ѧʽΪ ��
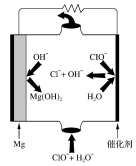
��4����þ-�������Ρ�ȼ�ϵ�ص�װ������ͼ��ʾ,�õ�ط�Ӧ�ĵ缫��Ӧʽ�ֱ�Ϊ���� �� ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и�����ѧ�ڵ�һ�ν��Բ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������Ԫ��A��B��C��D��E��ԭ������������������ֻ��C�ǽ���Ԫ�أ�B�ǵؿ��к�������Ԫ�أ�AԪ�س������ϼ�Ϊ+1�ͣ�1��A��C��������������ͬ��C��D��Ԫ��ԭ�ӵĵ�����֮��ΪA��B����Ԫ��ԭ�ӵĵ�����֮�͵�3��������������ȷ����
A��Ԫ�ص�ԭ�Ӱ뾶��A��B��C��D�� E
B����Ӧ�⻯������ȶ��ԣ�D > E
C��B��C��B��D�γɵĻ������л�ѧ��������ͬ
D������Ԫ��������������Ӧ��ˮ����������ǿ����E
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и�����ѧ�ڵ�һ�ν��Բ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£����и���������ָ����Һ��һ���ܴ����������
A����Al��Ӧ�ų�H2����Һ��Mg2����Ca2����HCO3����NO3��
B��10 mol��L��1��Ũ��ˮ��Al3����NH4����NO3����I��
C��0.1 mol��L��1KMnO4��Һ��Na����Fe2����SO42����Cl��
D��c(H��)/c(OH��)��1��10��12����Һ��K����Na����AlO2����CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������һ�С�������ѧ�������ϵ��л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͼװ�ã��г֡�����װ�����ԣ��������飬�Т���������֤ʵ���з�Ӧ��������

| ����ʵ�� | �������� |
A | ������ˮ�������� | ����ˮð�� |
B | ����NH4Cl��Ca(OH)2�Ļ���� | ��̪��Һ��� |
C | NaHCO3�������ȷֽ� | ����ʯ��ˮ����� |
D | ʯ���������Ƭ�����ȷֽ� | Br2��CCl4��Һ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ȷ�������з�Ӧԭ�������ӷ���ʽ��
A����С�մ�����θ����ࣺCO32- + 2H+ === CO2�� + H2O
B����������Һ�еμ�Ba(OH)2��Һ��Al3+�պó�����ȫ��
2Al3+ + 3SO42- + 3Ba2+ + 6OH- === 3BaSO4�� + 2Al(OH)3��
C������ʯ���ڴ����У�CaCO3 + 2H+ === Ca2+ + CO2�� + H2O
D��ϡ�����м�����������ۣ�Fe + 4H+ + NO3�� === Fe2+ + NO�� + 2H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com