
| A. | 使酚酞变红的溶液:K+、Na+、NO3-、Cl- | |
| B. | 无色透明的酸性溶液:MnO4-、K+、C1-、SO42- | |
| C. | 滴加KSCN显红色的溶液:NH4+、K+、Cl-、I- | |
| D. | 0.1 mol•L-1NaHCO3溶液:Na+、Ba2+、NO3-、OH- |
分析 A.使酚酞变红的溶液呈碱性,溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
B.无色溶液中不存在有色的高锰酸根离子;
C.滴加KSCN显红色的溶液中存在铁离子,铁离子能够氧化碘离子;
D.碳酸氢钠与氢氧根离子反应.
解答 解:A.使酚酞变红的溶液中存在大量氢氧根离子,K+、Na+、NO3-、Cl-之间不发生反应,都不与氢氧根离子反应,在溶液中能够大量共存,故A正确;
B.MnO4-为有色离子,在溶液中不能大量存在,故B错误;
C.滴加KSCN显红色的溶液中存在铁离子,铁离子具有强氧化性,能够氧化I-,故C错误;
D.NaHCO3与OH-发生反应,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 医疗上常用碳酸钡作X射线透视肠胃的内服药剂,即钡餐 | |
| B. | 石油的分馏产品如汽油、煤油、柴油等都是纯净物 | |
| C. | 食物的变质腐败属于吸热过程 | |
| D. | 硅的提纯与应用,促进了半导体元件与集成芯片的发展 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题


查看答案和解析>>
科目:高中化学 来源: 题型:实验题
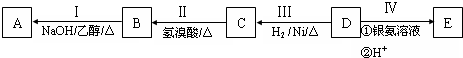
 ;
; 和
和 ;
;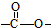 结构的有12种;E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为
结构的有12种;E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
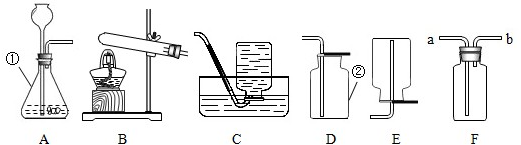
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向稀HNO3中滴加 Na2SO3溶液:SO32-+2H+=SO2↑+H2O | |
| B. | 向Na2SiO3溶液中通入过量SO2:SiO32-═SO2+H2O | |
| C. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O=4Na++2Cu (OH)2↓+O2↑ | |
| D. | 向A12(SO4)3溶液中加入过量的NO3•H2O:Al3++4 NH3•H2O=[A1(OH)4]-+4NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
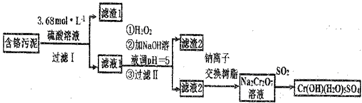
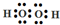 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 | |
| B. | 可用25mL碱式滴定管量取20.00 mLKMnO4溶液 | |
| C. | 用苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出 | |
| D. | 向乙酸乙酯中加入饱和Na2CO3溶液,振荡,分液除去乙酸乙酯中的少量乙酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com