
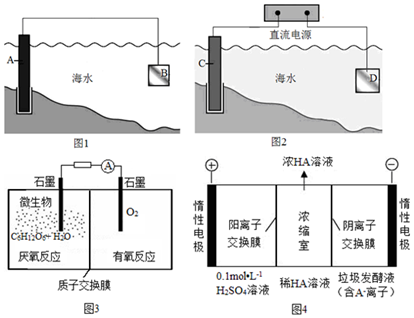
���� ��1���γ�ԭ���ʱ��Fe�������������������Ա�Feǿ�Ľ���������������ʴ��Fe��������������������������ʧ������������������������ʪ��ĵ��۵⻯����ֽ��
��2������ͼ֪��������C6H12O6ʧ���ӣ�������O2�õ��Ӻ�H+��Ӧ����ˮ�������ĵ缫��ӦʽΪC6H12O6+6H2O-24e-=6CO2+24H+�������ĵ缫��ӦʽΪO2+4e-+4H+�T2H2O��
��3���ٵ���������������������ʧ��������������
�ڸ��ݵ����������ƶ��������ش��жϣ�
��� �⣺��1���γ�ԭ���ʱ��Fe����������������Ҫѡ������Ա�Feǿ�Ľ���������������ѡп��Fe�����������������բ��C������������Ȼ�����Һʱ������������ʧ����������������缫��ӦΪ��2Cl--2e-�TCl2��������������ʪ��ĵ��۵⻯����ֽ������ʪ��ĵ��۵⻯����ֽ����������������ֽ������֤�������������ʴ�Ϊ��a������2Cl--2e-�TCl2����ʪ��ĵ��۵⻯����ֽ����������������ֽ������֤������������
��2������ͼ֪��������C6H12O6ʧ���ӣ�������O2�õ��Ӻ�H+��Ӧ����ˮ�������ĵ缫��ӦʽΪC6H12O6+6H2O-24e-=6CO2+24H+�������ĵ缫��ӦʽΪO2+4e-+4H+�T2H2O���ʴ�Ϊ��O2+4e-+4H+�T2H2O��
��3���������������������������ӷ���ʧ���ӵ�������Ӧ���缫��ӦʽΪ��4OH--4e-�T2H2O+O2�����ʴ�Ϊ��4OH--4e-�T2H2O+O2����
���ڵ��ص���������OH-�ŵ磬����c��H+��������H+������ͨ�������ӽ���Ĥ����Ũ���ң����ݵ��ԭ���������е�������������������A-ͨ�������ӽ���Ĥ����������Ũ���ң�������H++A-�THA������Ũ������
�ʴ�Ϊ������OH-�ŵ磬c��H+������H+������ͨ�������ӽ���Ĥ����Ũ���ң�A-ͨ�������ӽ���Ĥ����������Ũ���ң�H++A-�THA������Ũ������
���� �����漰���غ�ԭ��صĹ���ԭ���Լ�Ӧ�õĿ��飬ע��֪ʶ��Ǩ�ƺ�Ӧ���ǽ���Ĺؼ���ע�����ԭ��غ͵��������ӵ��ƶ��������ջ����ǹؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
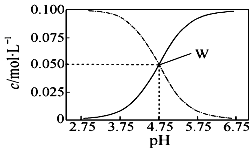 25�棬��c��CH3COOH��+c��CH3COO-��=0.1mol•L-1��һ�����ʹ����ƻ����Һ����Һ��c��CH3COOH����c��CH3COO-����pHֵ�Ĺ�ϵ��ͼ��ʾ�������й�����Ũ�ȹ�ϵ������ȷ���ǣ�������
25�棬��c��CH3COOH��+c��CH3COO-��=0.1mol•L-1��һ�����ʹ����ƻ����Һ����Һ��c��CH3COOH����c��CH3COO-����pHֵ�Ĺ�ϵ��ͼ��ʾ�������й�����Ũ�ȹ�ϵ������ȷ���ǣ�������| A�� | pH=5.5��Һ�У�c��CH3COOH����c��CH3COO-����c��H+����c��OH-�� | |
| B�� | pH=3.5��Һ�У�c��Na+��+c��H+��+c��OH-��+c��CH3COOH��=0.1mol•L-1 | |
| C�� | ���¶��´���ĵ���ƽ�ⳣ��Ϊ10-4.75 | |
| D�� | ��W������ʾ��Һ�м���������0.05 mol•L-1NaOH��Һ��c��H+��=c��CH3COOH��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 | B�� | 2 | C�� | 3 | D�� | 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ĵ绯��ʴ�Ȼ�ѧ��ʴ�ձ� | B�� | �����ڸ�������ﲻ��ʴ | ||
| C�� | ������í�������壬�����ױ���ʴ | D�� | ԭ��ص�·�е����ɸ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼���� | B�� | �������� | C�� | ������ | D�� | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ȶ��ԣ�Na2CO3��NaHCO3 | |
| B�� | ��ͬ�¶�ʱ��ˮ���ԣ�Na2CO3��NaHCO3 | |
| C�� | �����ʵ���Ũ�ȵ���Һ�ļ��ԣ�Na2CO3��NaHCO3 | |
| D�� | ��ͬŨ�ȵ����ᷴӦ�ľ��ҳ̶ȣ�Na2CO3��NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����FeCl3��Һ��Ӧ��Fe+Fe3+�T2Fe2+ | |
| B�� | Fe�����ᷴӦ��2Fe+6H+�T2Fe3++3H2�� | |
| C�� | FeCl2��Һ��Cl2��Ӧ��Fe2++Cl2�TFe3++2Cl- | |
| D�� | Fe��OH��3�����ᷴӦ��Fe��OH��3+3H+�TFe3++3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������������ƣ����£� | B�� | �����������������ƣ����£� | ||
| C�� | ����������̼�����£� | D�� | ����������ŨHNO3�����£� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
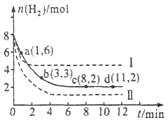 ��ҵ����һ����CO2�������״�ȼ�ϵķ�����CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ•mol-1
��ҵ����һ����CO2�������״�ȼ�ϵķ�����CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ•mol-1�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com