
 mol
mol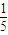
 =
=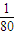 mol(L?s),故A错误;
mol(L?s),故A错误;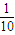 ,为0.03mol/L,但减小压强平衡逆向进行,Z的平衡浓度小于0.03mol/L,故B错误;
,为0.03mol/L,但减小压强平衡逆向进行,Z的平衡浓度小于0.03mol/L,故B错误;

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| 反应时间/min | n(SiF4)/mol | n(H2O)/mol |
| 0 | 1.20 | 2.40 |
| t1 | 0.80 | a |
| t2 | b | 1.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 一定条件下,体积为2L的密闭容器中,1mol A和1mol B进行反应:A(g)+3B(g)?2C(g)经2分钟反应达到平衡,此时生成0.2mol C.下列说法正确的是( )
一定条件下,体积为2L的密闭容器中,1mol A和1mol B进行反应:A(g)+3B(g)?2C(g)经2分钟反应达到平衡,此时生成0.2mol C.下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:


 ,判断其中的化学键的类型
,判断其中的化学键的类型查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2013届湖南省、四中)两校联考高一下学期期末考试化学 题型:实验题
主族元素A、B、C、D、E的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且C最外层电子数是次外层电子数的2倍。A、B单质在常温下均为气体,它们在一定条件下以体积比2∶1完全反应,生成物在常温下是液体F。此液体与D单质能激烈反应生成A的单质,所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子。E的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水。回答下列问题:
⑴写出元素符号A , C 。
⑵E元素的最高价氧化物和盐酸反应的离子方程式为 : 。
⑶用电子式表示F的形成过程 。
在加热的条件下B、D形成的化合物的电子式为 ,其中的化学键的类型为 。
⑷写出一种有A、B、C、D组成的化合物的化学式 。
(5)B的气态氢化物是天然气的主要成分,它的空间结构为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com