
| A. | 纯净空气 | B. | 鸡蛋清水溶液 | C. | 牛奶 | D. | 淀粉溶液 |
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 盐酸、氢氧化钠醋酸、干冰 | B. | 澄清的石灰水、铜、氨气 | ||
| C. | 石油、水、硫酸钡 | D. | 海水、氯化钠、氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
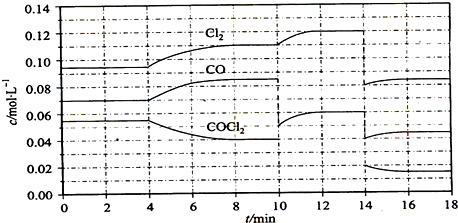
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
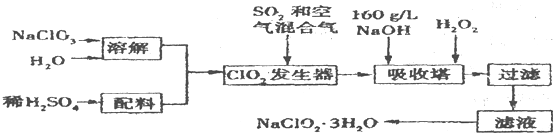
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气的CCl4溶液不能使干燥红色布条褪色 | |
| B. | 通过化学变化可以实现16O与18O间的相互转化 | |
| C. | 为了便于运输和使用,可以将液氯储存在钢瓶(主要成分为铁)中 | |
| D. | 700℃时,4Na+CCl4=C+4NaCl,该反应属于置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1000 mL,212 g | B. | 950 mL,201.4 g | C. | 500 mL,286 g | D. | 1000 mL,201.4 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓ | |
| B. | 碳酸钠溶液与石灰乳的反应:CO32-+Ca2+═CaCO3↓ | |
| C. | 盐酸与氢氧化铁反应:3H++Fe(OH)3=Fe3++3H2O | |
| D. | NaOH溶液中加入醋酸:OH-+H+=H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 漂白粉在空气中不稳定,可用于漂白纸张 | |
| B. | 氨气具有还原性,可用作制冷剂 | |
| C. | Na2O2呈浅黄色,可用作潜水艇中的供氧剂 | |
| D. | 氧化铝的熔点高,可用于制造耐火材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com