
对元素周期表和元素周期律的发现有突出贡献的科学家是( )
A. 拉瓦锡 B. 阿伏加德罗 C. 门捷列夫 D. 道尔顿
 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
已知X,Y,Z,W四种短周期元素的原子序数依次增大,其中X与Y、Z、W所形成的常见化合物(10e或18e)在常温下均为气态,在元素周期表中Z与W相邻,Y的最高价氧化物的水化物与其氢化物反应生成盐,且Y的核电荷数与W的最外层电子数相同.
(1)Z离子的结构示意图是 .
(2)X、Y、Z可组成一种化合物,原子个数比为4:1:1,该化合物的化学式是 ,其中含有的化学键有 .
(3)X与Y所形成的分子的电子式为 ,它比同主族其他元素的氢化物沸点高的原因是 .
(4)请设计一个简单的实验,说明Z、W两种元素非金属性的强弱,写出实验方法和现象: 向.
查看答案和解析>>
科目:高中化学 来源: 题型:
从我们熟悉的食盐、金属、冰到贵重的钻石等都是晶体,而同样透明的玻璃却是非晶体。下列关于晶体和非晶体的本质区别的叙述中,正确的是
A.是否具有规则的几何外形的固体
B.是否具有固定组成的物质
C.是否具有美观对称的外形
D.内部基本构成微粒是否按一定规律做周期性重复排列
查看答案和解析>>
科目:高中化学 来源: 题型:
W、M、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质之一。X的某一种单质在高空大气层中保护人类免遭太阳光中紫外线强烈侵袭;Y的基态原子核外有6个原子轨道处于半充满状态;Z能形成红色的Z2O和黑色的ZO两种氧化物。
(1)Y3+基态的电子排布式可表示为 。
(2)M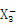 的空间构型 (用文字描述)。
的空间构型 (用文字描述)。
(3)M可形成多种氢化物,其中MH3的碱性强于M2H4的原因是_________________。
(4)根据等电子原理,WX分子的结构式为 。
(5)1 mol WX2中含有的σ键数目为 。
(6)H2X分子中X原子轨道的杂化类型为 。
(7)向Z2+的溶液中加入过量NaOH溶液,可生成Z的配位数为4的配位离子,写出该配位离子的结构式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
分类是学习和研究化学的一种重要方法,下列分类合理的是( )
A. K2CO3和K2O都属于盐
B. KOH和Na2CO3都属于碱
C. H2SO4和HNO3都属于酸
D. Na2O和Na2SiO3都属于氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3是一种重要的工业原料.下列关于合成氨的说法中,不正确的是( )
A. 工艺涉及催化技术
B. 工艺涉及高温高压技术
C. 原料之一的氮气来自空气
D. 从合成塔出来的气体中,氨的体积分数为100%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述或操作不正确的是( )
|
| A. | 浓硫酸具有强氧化性,稀硫酸无氧化性 |
|
| B. | 浓硫酸不慎沾到皮肤上,立即用大量的水冲洗 |
|
| C. | 稀释浓硫酸时应将浓硫酸沿着烧杯壁慢慢地注入盛有水的烧杯中,并不断搅拌 |
|
| D. | 浓硫酸与碳的反应中,浓硫酸仅表现强氧化性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com