
【题目】网络趣味图片“一脸辛酸”,是在人脸上重复画满了辛酸的键线式结构。下列有关辛酸的叙述正确的是

A. 辛酸的同分异构体中能水解生成乙醇的酯类同分异构体共有8种
B. 辛酸的同分异构体(CH3)3CCH(CH3)CH2COOH的名称为2,2,3——三甲基戊酸
C. 辛酸和油酸(C17H33COOH)都是一元羧酸,故二者属于同系物
D. 1mol辛酸与足量的Na反应产生11.2LH2
【答案】A
【解析】
A.辛酸的分子式为C8H16O2,能水解生成乙醇的同分异构体属于酯类,该同分异构体可写成C5H11-COOC2H5,因戊基(C5H11-)共有8种,所以符合条件的同分异构体共有8种,A项正确;
B.按系统命名法命名时要以包含羧基的最长碳链为主链,以羧基的碳为起点给主链编号,其名称为:3,4,4-三甲基戊酸,B项错误;
C.辛酸(C7H15COOH)的烃基是饱和链烃基,油酸(C17H33COOH)的烃基是不饱和的烯烃基,结构不相似,故二者不属于同系物,C项错误;
D. 1mol辛酸与足量的Na反应产生0.5mol氢气,因题目没有明确是标准状态,无法确定生成氢气的体积,D项错误;答案选A。


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯时,经过配制混酸、硝化反应(50~60℃)、洗涤分离、干燥蒸馏等步骤,下列图示装置和原理能达到目的的
A. 配制混酸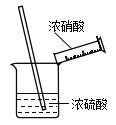 B. 硝化反应
B. 硝化反应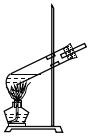
C. 分离硝基苯 D. 蒸馏硝基苯
D. 蒸馏硝基苯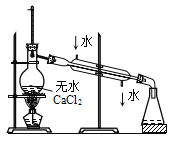
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁在工业、医疗等领域均有重要用途。某化学兴趣小组利用硼砂工厂的固体废弃物(主要含有MgCO3、MgSiO3、Al2O3和Fe2O3等),设计了如下回收镁的工艺流程:
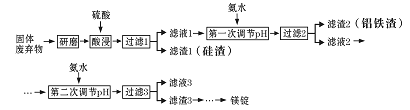
(1)酸浸前,将固体废弃物研磨的目的是___________________________________。为达到目的,还可以采取的措施是_________________________________________________(任写一条)。
(2)酸浸时,生成滤渣1的离子方程式为__________________________________。
(3)第一次调节pH的目的是_____________________________。当加入氨水使Al3+开始沉淀时,溶液中c(Fe3+)/c(Al3+)为__________________。已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.0×10-33,Ksp[Mg(OH)2]=1.8×10-11。
(4)设计简单方案分离滤渣2中的成分,简述实验过程:________________________________。
(5)滤液3中可回收利用的物质主要是__________(写化学式),其阳离子的电子式为________。
(6)写出工业上从滤渣3中获得镁锭的所有反应的化学方程式:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:X为具有浓郁香味、不易溶于水的油状液体,食醋中约含有3%~5%的D,其转化关系如下图所示。
请回答:

(1)X的结构简式是__________________。
(2)A→B的化学方程式是____________________________________________。
(3)X+H2O→A+D的化学方程式是____________________________________________。
(4)下列说法不正确的是________。
A A+D→X的反应属于加成反应
B A与金属钠反应比水与金属钠反应要剧烈得多
C 除去X中少量D杂质可用饱和Na2CO3溶液
D 等物质的量的A、B、D完全燃烧消耗O2的量依次减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2SO2(g) + O2(g) ![]() 2SO3(g) △H =-akJ/mol(a>0),能量变化如图所示,下列说法不正确的是
2SO3(g) △H =-akJ/mol(a>0),能量变化如图所示,下列说法不正确的是

A. 2SO2(g) +O2(g) ![]() 2SO3(1) △H>-a kJ/mol
2SO3(1) △H>-a kJ/mol
B. 过程II可能使用了催化剂,使用催化剂不可以提高SO2的平衡转化率
C. 反应物断键吸收能量之和小于生成物成键释放能量之和
D. 将2molS02(g)和1 mol 02(g)置于一密闭容器中充分反应后放出的热量小于a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ:下列各项分别与哪个影响化学反应速率因素的关系最为密切?
(1)夏天的食品易变霉,在冬天不易发生该现象_____;
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢_____;
(3)MnO2加入双氧水中放出气泡更快_____.
Ⅱ:在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
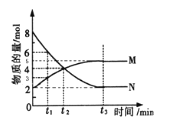
(1)比较t2时刻,正逆反应速率大小V正______V逆.(填“>”、“=”、“<”)
(2)若t2=2min,计算反应开始至t2时刻用M的浓度变化表示的平均反应速率为:_____.
(3)t3时刻化学反应达到平衡,反应物的转化率为_____.
(4)如果升高温度,则V逆_____(填增大、减小或不变).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.1 mol/LNaOH溶液分别滴加到0.1 mol/LHA溶液和HB溶液中,两混合溶液中离子浓度与pH的变化关系如图所示,回答下列问题:
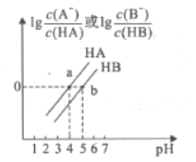
(1)请计算出Ka(HA) =_____,Ka(HB)_____ Ka(HA) (填“大于' “等于”或“小于”)。
(2)等浓度的HA和HB溶液,若要向其中之一加水让二者pH值相等,应该向_____中加水。
(3)若分别向等浓度等体积的HA和HB溶液中加入NaOH固体让二溶液都呈中性,则 ______需要的NaOH多。
(4)a点溶液中,水电离出的c(H+)=_______。b点溶液中,c(B-)____ c(Na+)(填“大于”、“等于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,能表示反应X(g)+2Y(g)![]() 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
① X、Y、Z的物质的量之比为1:2:2 ② X、Y、Z的浓度不再发生变化
③ X、Y、Z的浓度相等时 ④ 单位时间内消耗nmolX,同时生成2nmolZ
⑤ 2υ正(X)=υ逆(Y) ⑥ 容器中的压强不再发生变化
⑦ 密闭容器内气体的密度不再变化 ⑧ 密闭容器内气体的平均相对分子质量不再变化
A. ③⑤⑥⑦ B. ①③④⑦
C. ②④⑧ D. ②⑤⑥⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com