
A、 |
B、 |
C、 |
D、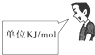 |
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
| A、元素的第一电离能是元素的单质失去最外层1个电子所需要吸收的能量,同周期从左到右元素的电离能逐渐增大 |
| B、元素的电负性是衡量元素在化合物中吸引电子能力大小的一种标度,同主族从上到下元素的电负性逐渐减小 |
| C、元素的性质随着原子序数的增大而呈周期性变化 |
| D、鲍林的电负性是以氟的电负性为4.0和锂的电负性为1.0作为相对标准得出的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下可发生反应2M2++Z2═2M3++2Z- |
| B、还原性强弱顺序为:X2+<Z-<R-<M2+ |
| C、Z元素在反应①中被氧化,在③中被还原 |
| D、氧化性强弱顺序为:XO4-<Z2<R2<M3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
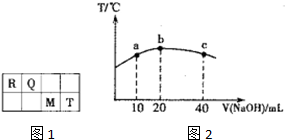 短周期元素R、Q、M、T在元素周期表中的相对位置如图1,已知R原子最外层电子数与次外层电子数之比为2:1.
短周期元素R、Q、M、T在元素周期表中的相对位置如图1,已知R原子最外层电子数与次外层电子数之比为2:1.| +X |
| +X |
| 化合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com