
【题目】一定温度下,在一个容积为5L的密闭容器中,充入氨和氧气,它们的物质的量之比为1:2,发生反应:
4NH3+5O24NO+6H2O(g);△H<0
(1)在达到平衡后,加入相当于原组成气体1倍的惰性气体,如果容器的容积不变,平衡移动;如果总压强保持不变,平衡移动.
(2)升高温度平衡移动.
(3)加入催化剂,NH3的转化率 ,
(4)上述反应在一定条件下2min后达到平衡,若充入的NH3为2mol,NH3的转化率为20%,以NO的浓度变化表示该反应的平均反应速率为 . O2的平衡浓度为 .
【答案】
(1)不;正方向
(2)逆方向
(3)不变
(4)0.25mol?L﹣1?min﹣1;0.875mol?L﹣1
【解析】解:(1)如果容器的容积不变,各组分的浓度不变,平衡不移动,如果总压强不变,充入惰性气体,体积扩大,相当于减小压强,平衡正向移动,所以答案是:不;正方向;(2)升高温度平衡向吸热反应方向移动,向逆反应方向移动,所以答案是:逆方向;(3)加入催化剂,平衡不移动,所以NH3的转化率不变,所以答案是:不变;(4)设充入NH3为xmol,
4NH3(g)+ | 5O2(g) | 4NO(g)+ | 6H2O(g) | |
加入量 | x | 2x | 0 | 0 |
反应量 | 0.2x | 0.25x | 0.2x | 0.3x |
平衡量 | 2 | 2x-0.25x | 0.2x | 0.3x |
2min后达到平衡,NH3为2mol,NH3的转化率为20%,
x﹣0.2x=2,
解得x=2.5
用NO的浓度变化表示该反应的平均反应速率为 ![]() =0.25molL﹣1min﹣1 ,
=0.25molL﹣1min﹣1 ,
O2的平衡浓度为 ![]() =0.875molL﹣1 ,
=0.875molL﹣1 ,
所以答案是:0.25molL﹣1min﹣1;0.875molL﹣1 .
【考点精析】认真审题,首先需要了解化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)).


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下图曲线表示物质A生成物质P的化学反应,在无催化条件和有酶催化条件下的能量变化过程。下列相关叙述中正确的是

A.ab段表示在有酶催化条件下,使物质A生成物质P反应发生需要的活化能
B.bd段表示在无催化剂催化条件下,使物质A生成物质P反应发生需要的活化能
C.若将酶催化改为无机催化剂催化该反应,则b在纵轴上将向下移动
D.酶可通过降低反应的活化能来加快反应的进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1994年科学家发现一种元素,它的核内有161个中子,质量数为272,该元素原子序数是( )
A. 111B. 161C. 272D. 443
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体组成结构的叙述中,正确的是( ) 
A.SiO2晶体中最小环上的原子数为6
B.在晶体中只要有阳离子就一定有阴离子
C.12g石墨烯(如图1)中含有六元环的个数为0.5NA
D.720g C60晶体(如图2)中含有0.5NA个晶胞结构单元
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在量热器中将50mL,0.50molL﹣1CH3COOH溶液与50mL、0.55molL﹣1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J0C﹣1 , C=4.18Jg﹣10C﹣1 , 溶液的密度为1gcm﹣3 . 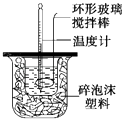
(1)试求CH3COOH的“中和热”.
(2)请你分析(1)中测得的实验值偏差可能是什么原因造成的? .
(3)若HNO3 (aq)+NaOH(aq)=NaNO3(aq)+H2O(l);△H=﹣57.3KJmol﹣1;
现有①稀H2SO4与Ba(OH)2(aq) ②浓H2SO4与Ba(OH)2(aq)
③HNO3与Ba(OH)2(aq)反应生成1molH2O(l) 的反应热分别为△H1、△H2、△H3 ,
则△H1、△H2、△H3三者由小到大的关系为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼(BCl3)是一种重要的化工原料,可用于制取乙硼烷(B2H6),也可作有机合成催化剂.某兴趣小组拟选用下列装置制备BCl3(已知BCl3的沸点为12.5℃,熔点为﹣107.3℃;2B+6HCl ![]() 2BCl3↑+3H2↑.
2BCl3↑+3H2↑. 
请回答下列问题:
(1)装置B中发生反应的化学方程式为 .
(2)按气流方向连接各装置的接口,顺序为a﹣﹣﹣﹣﹣﹣﹣f﹣g﹣h.连接好装置后的实验操作是 .
(3)装置D的作用是;实验中若不用装置C,可能产生的危险是 .
(4)BCl3遇水发生水解观察到大量的白雾,生成两种酸,其反应的化学方程式为: .
(5)装置E的作用除了可以吸收多余Cl2外,还起到的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数,下列有关叙述正确的是
A.SiO2的摩尔质量为60
B.过量的Fe粉与1 mol Cl2充分反应转移的电子数目为2NA
C.常温下,pH=2的NaHSO4溶液中所含H+数目为0.01NA
D.标准状况下,2.24 L HF与1.8 g H2O所含电子数目均为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式正确的是( )
A.CuCl2═Cu2++Cl2﹣
B.Al2(SO4)3=2Al3++3SO ![]()
C.Fe2(SO4)3═2Fe2++3SO ![]()
D.Ba(NO3)2═Ba2++2(NO3)2﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com