

分析 废副产物硫酸亚铁溶液(含TiO2+离子)加铁屑、氯化钙、水蒸气加热,同时水蒸气还可以搅拌反应物,使反应物充分反应,铁粉与废液中的硫酸发生置换反应,与少量的铁离子发生化合反应,在加热条件下TiO2+水解生成Ti(OH)4,钙离子与硫酸根离子结合生成CaSO4•2H2O,都是复分解反应,过滤,滤渣为Ti(OH)4、CaSO4•2H2O,TiO2•xH2O,滤液主要含有FeCl2,滤液中通入空气同时加入石灰乳,再用水蒸气加热,亚铁离子部分被空气中氧气氧化成铁离子,通过压滤机得滤渣2主要为氢氧化亚铁和氢氧化铁的混合物,滤液中主要含有CaCl2可循环利用,滤渣2在65℃条件下加热可得氧化铁黑(Fe3O4),据此答题.
解答 解:硫酸亚铁溶液(含TiO2+离子)加铁屑、氯化钙、水蒸气加热,同时水蒸气还可以搅拌反应物,使反应物充分反应,在加热条件下TiO2+水解生成Ti(OH)4,钙离子与硫酸根离子结合生成CaSO4•2H2O,过滤,滤渣为Ti(OH)4、CaSO4•2H2O,TiO2•xH2O,滤液主要含有FeCl2,滤液中通入空气同时加入石灰乳,再用水蒸气加热,亚铁离子部分被空气中氧气氧化成铁离子,通过压滤机得滤渣2主要为氢氧化亚铁和氢氧化铁的混合物,滤液中主要含有CaCl2可循环利用,滤渣2在65℃条件下加热可得氧化铁黑(Fe3O4),
(1)根据上面的分析可知,沉淀池产生的滤渣除了Ti(OH)4外,主要成分是CaSO4•2H2O,沉淀池产生Ti(OH)4的离子方程式为 TiO2++3H2O=Ti(OH)4↓+2H+(或Fe+TiO2++3H2O=Ti(OH)4↓+Fe2++H2↑ ),
故答案为:CaSO4•2H2O; TiO2++3H2O=Ti(OH)4↓+2H+(或Fe+TiO2++3H2O=Ti(OH)4↓+Fe2++H2↑ );
(2)根据上面的分析可知,沉淀池中发生的反应有化合、置换、复分解,没有发生分解反应,故选C;
(3)氧化桶中发生的主要反应是生成氢氧化亚铁,然后空气中氧气将氢氧化亚铁氧化成氢氧化铁,反应的化学方程式为Fe2++2OH-=Fe(OH)2↓、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:Fe2++2OH-=Fe(OH)2↓、4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)由于Fe2+容易被氧化,所以氧化桶流出的滤液中Fe3+和Fe2+的比例略小于2:1,约为1.9:1,
故答案为:Fe2+容易被氧化,应使其比例略高;
(5)沉淀池、氧化桶中通入的水蒸气除了加热升温加快反应外,还可以搅拌反应物,使反应物充分反应,
故答案为:搅拌反应物,使反应物充分反应;
(6)滤液中主要含有CaCl2,最佳处理方式是循环至沉淀池继续使用,
故答案为:循环至沉淀池继续使用;
(7)根据上面的分析可知,流程中可在热交换器中预热的物质是水、FeCl2溶液,
故答案为:水、FeCl2溶液.
点评 本题考查了物质制备方案的设计方法,题目难度中等,明确制备原理及常见物质的性质为解答关键,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及化学实验、化学计算能力.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 化学反应的速率和限度均可通过改变化学反应条件而改变 | |
| C. | 可逆反应只是代表少数反应 | |
| D. | 化学反应达到平衡状态时,正反应速率与逆反应速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
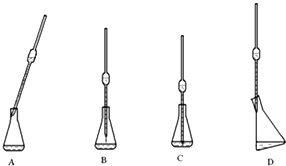 利用所学化学知识解答问题:
利用所学化学知识解答问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
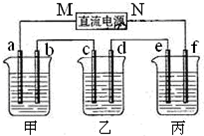
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
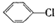 制备
制备 步骤:
步骤: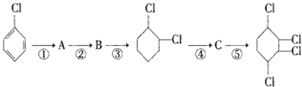
 ,B
,B ,C
,C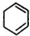
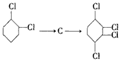 的化学方程式①
的化学方程式①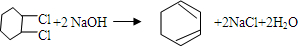 ②
②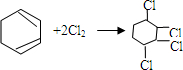 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:6 | B. | 6:1 | C. | 1:5 | D. | 5:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com